时间:2017-08-08 03:53:09
1、选择题 能证明氮元素比磷元素非金属性强的事实是
[? ]
A.氮气在常温下是气体,而磷的单质是固体
B.N2不能在空气中燃烧,而磷能在空气中燃烧
C.NH3极易溶于水,而PH3难溶于水
D.NH3在空气中不可燃,而PH3可燃?
参考答案:D
本题解析:
本题难度:一般
2、选择题 原子序数从11依次增加到17,下列递变关系中错误的是?
[? ]
A.最外层电子数逐渐增大?
B.原子半径逐渐增大
C.最高正化合价逐渐增大?
D.从Si到Cl,最低负化合价从-4到-1
参考答案:B
本题解析:
本题难度:一般
3、选择题 已知A、B、C、D、F是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是
[? ]
A. 原子半径:C>D>A>B
B. C和E的单质可通过电解饱和的CE水溶液获得
C. C与B形成的两种化合物中化学键类型完全相同
D. A、D、E最高价氧化物对应水化物的酸性逐渐增强
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列叙述中错误的是
[? ]
A.136C和146C属于同一种元素,它们互为同位素 ?
B.11H和21H是不同的核素,它们的质子数相等 ?
C.146C和147N的质量数相等,它们的中子数不等 ?
D.63Li和73Li的电子数相等,中子数也相等
参考答案:D
本题解析:
本题难度:简单
5、填空题 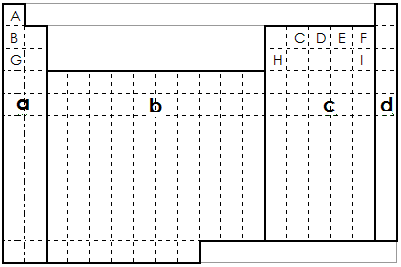
(1)在上面元素周期表中全部是金属元素的区域为__________。
(A)a (B)b (C)c (D)d
(2)G元素与E元素形成的化合物的化学式是__________、__________,它们都是__________(填“共价化合物”或“离子化合物”)。表格中十种元素的最高价氧化物对应的水化物中,碱性最强的是
__________(用化合物的化学式表示,下同),酸性最强的是__________,属于两性氢氧化物的是
__________。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是_________(填名称),可以验证该结论的实验是_________。(填编号)
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
参考答案:(1)b
(2)Na2O2;Na2O;离子化合物;NaOH;HClO4;Al(OH)3(3)①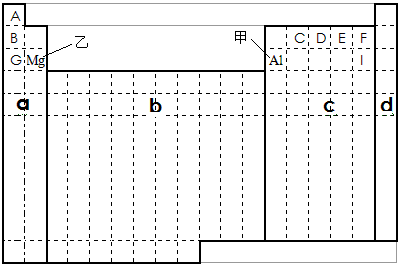 ②乙或镁;bc
②乙或镁;bc
本题解析:
本题难度:一般