时间:2017-08-08 03:44:20
1、选择题 常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是
A.pH > 7,且c(OH-) > c(Na+) >c(H+) >c(CH3COO-)
B.pH > 7,且c(Na+) + c(H+) = c(OH-) + c(CH3COO-)
C.pH < 7,且c(CH3COO-) >c(H+) > c(Na+) > c(OH-)
D.pH = 7,且c(CH3COO-) = c(Na+) > c(H+) = c(OH-)
参考答案:A
本题解析:正确答案:A
A、违背电荷守恒规律;B、电荷守恒; C、正确;D、由电荷守恒c(Na+) + c(H+) = c(OH-) + c(CH3COO-),可知,中性时,c(CH3COO-) = c(Na+) > c(H+) = c(OH-)
本题难度:困难
2、选择题 下列物质中属于电解质的是
A.钠
B.蔗糖
C.盐酸
D.氯化钠
参考答案:D
本题解析:溶于水或熔融状态下能电离出离子的混合物是电解质,所以选项D正确。A是单质。C是混合物,不符合。蔗糖是非电解质,不正确,答案选D。
本题难度:简单
3、选择题 下列各组溶液之间的反应,所用离子方程式表示相同的是( )
A.硝酸钡与稀硫酸,氯化钡与硫酸钠
B.盐酸与碳酸钠,盐酸与碳酸氢钠
C.氢氧化钠与硫酸,氢氧化钡与硫酸
D.氢氧化钠与盐酸,氢氧化钾与醋酸
参考答案:A
本题解析:A选项均可用Ba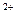 +SO
+SO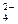
 BaSO
BaSO ↓表示;B选项中CO
↓表示;B选项中CO 和HCO
和HCO 书写形式不同;C选项中氢氧化钡和硫酸反应,Ba
书写形式不同;C选项中氢氧化钡和硫酸反应,Ba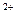 和SO
和SO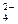 也参与了反应;D选项中醋酸是弱酸,应以化学式表示。
也参与了反应;D选项中醋酸是弱酸,应以化学式表示。
本题难度:一般
4、选择题 下列反应的离子方程式书写正确的是( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3・H2O=AlO2―+4NH4++2H2O
B.浓烧碱溶液中加入铝片:Al+2OH-=AlO2―+H2↑
C.用浓NaOH溶液溶解Al2O3:2OH-+Al2O3=2AlO2―+H2O
D.往碳酸镁中滴加稀盐酸:CO32―+2H+=CO2↑+H2O
参考答案:C
本题解析:A中应生成Al(OH)3而不是AlO2―,因为Al(OH)3不溶于氨水;B中电荷不守恒;D中MgCO3难溶,不能拆写为CO32―。
本题难度:简单
5、选择题 下列反应的离子方程式正确的是?(?)
A.苯酚钠溶液中通入少量CO2:CO2 + H2O + C6H5O-→C6H5OH + HCO3-
B.浓盐酸与MnO2反应制取氯气:MnO2+2H++2Cl-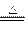 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C.向NaAlO2溶液中通入少量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
D.用惰性电极电解氯化镁溶液:2Cl-+ 2H2O 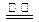 H2↑+ Cl2↑+2OH-
H2↑+ Cl2↑+2OH-
参考答案:A
本题解析:A项苯酚钠溶液中通入CO2反应的离子方程式与CO2通入的量无关,无论少量还是过量均为CO2 + H2O + C6H5O-= C6H5OH + HCO3-;B项电荷及元素均不守恒;C项应该生成CO32-;D项应该有Mg(OH)2↓生成。
本题难度:简单