时间:2017-08-06 11:20:19
1、选择题 有一铁的氧化物样品,用140mL5mol?L-1盐酸可恰好使其完全溶解.所得溶液可吸收标准状况下0.56L氯气,使其中的Fe2+全部转化为Fe3+.该样品可能的化学式为( )
A.Fe4O5
B.Fe5O7
C.Fe2O3
D.Fe3O4
参考答案:B
本题解析:
本题难度:一般
2、选择题 某氧化剂中,起氧化作用的是X2O72-,在溶液中0.2mol该离子恰好能使0.6mol?SO32-离子完全氧化,则X2O72-离子被还原后的化合价为( )
A.+1
B.+2
C.+3
D.+4
参考答案:C
本题解析:
本题难度:一般
3、选择题 在KI和KIO3混合溶液中加入稀硫酸,发生反应,生成碘、硫酸钾和水。此反应中被氧化的碘元素与被还原的碘元素的物质的量比正确的是
A.5∶1
B.2∶1
C.1∶3
D.1∶5
参考答案:A
本题解析:本题中KI和KIO3中I元素化合价都归中为零,由得失电子守恒可知被氧化碘元素与被还原的碘元素的物质的量比为5︰1。
本题难度:一般
4、选择题 用足量的CO还原32.0 g某种氧化物,将生成的气体通入足量澄清石灰水中,得到60 g沉淀,则该氧化物是
[? ]
参考答案:B
本题解析:
本题难度:一般
5、选择题 我校化学兴趣小组做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色。则该条件下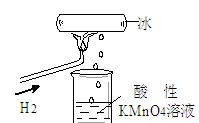
A.生成的水分子化学性质比较活泼
B.H2燃烧生成了具有氧化性的物质
C.H2燃烧的产物中可能含有一定量的H2O2
D.H2被冷却为液态氢,液氢的水溶液具有还原性
参考答案:C
本题解析:从反应现象可看出,生成了一种物质:既具有氧化性又具有还原性:2MnO + 5H2O2+ 6H+= 2Mn2++ 5O2↑+8H2O和H2O2+2H+ +2Fe2+=2Fe3++2H2O,答案为C
+ 5H2O2+ 6H+= 2Mn2++ 5O2↑+8H2O和H2O2+2H+ +2Fe2+=2Fe3++2H2O,答案为C
本题难度:简单