时间:2017-08-06 11:15:35
1、填空题 铬铁矿的主要成分可表示为FeO・Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示。 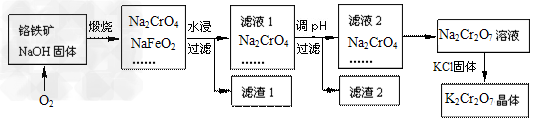
已知:①?NaFeO2遇水强烈水解。?②2CrO42-?+?2H+?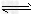 Cr2O72-+?H2O ?
Cr2O72-+?H2O ?
请回答:?
(1)K2Cr2O7中Cr元素的化合价是________________。
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是_____________________。
(3)滤渣1为红褐色的固体,滤渣1的成分是(填名称)______________,滤液1的成分除Na2CrO4、NaOH外,还含有(填化学式)______________。
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,电解时阴极的电极反应式为____________________。
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是___________________。
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
_________、过滤、洗涤、干燥。
2、填空题 工业上生产高氯酸(沸点:90℃)时还同时生产了亚氯酸钠,其工艺流程如下:? 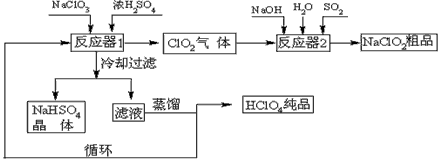
(1)冷却过滤的目的是降低NaHSO4的_________并分离出NaHSO4晶体。
(2)反应器2中发生反应的离子方程式为___________。SO2的作用是作___________剂。
(3)循环使用的物质是_____________。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是_____________。
(5)工业上用铂作阳极、铜或银作阴极电解盐酸也可制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)________________。
3、填空题 某地有软锰矿和闪锌矿两座矿山,它们的组成如下:软锰矿:MnO2含量≥65 %,SiO2含量约为20%,
Al2O3含量约为4%,其余为水分;闪锌矿:ZnS含量≥ 80%,FeS、CuS、SiO2含量约为7%,其余为水分。科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如下图所示。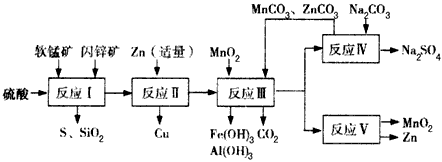
请回答下列问题:
(1)反应I后过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等。试写出反应I中生成
CuSO4的化学方程式_____________________。
(2)反应Ⅱ加入适量锌的作用是________________________。如果锌过量,还会进一步发生反应的离子方程式为________________________。
(3)反应V的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为____________。
(4)本工艺所用的原料除软锰矿、闪锌矿、硫酸外还需要________等原料。
4、填空题 工业上制备BaCl2的工艺流程图如下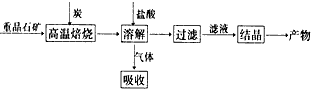
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得 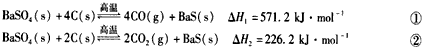
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为__________________
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时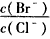 =___________
=___________
[ Ksp(AgBr) =5. 4×10-13,Ksp(AgCl) = 2. 0×10-10]
(3)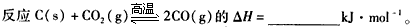
(4)买际生产中必须加入过量的炭,同时还要通入空气,其目的是_____________________
5、填空题 工业上用铜屑和浓硝酸为原料制取硝酸铜。在实际生产中,需把浓硝酸用等体积的水稀释。试简要回答下列问题:
(1)用稀硝酸而不用浓硝酸的原因是___
(2)从经济效益和环境保护角度考虑,设计制取硝酸铜最适宜的方法,用化学方程式表示为____