时间:2017-08-06 11:08:36
1、填空题 如图,A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。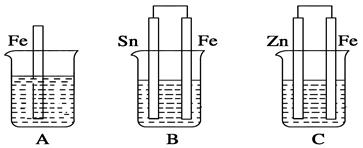
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________。
(3)C中被腐蚀的金属是________,总反应的化学方程式为_____________________。比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为__________。
(填序号)。
参考答案:(1)Fe+2H+=Fe2++H2↑
(2)2H++2e-=H2↑
(3)Zn Zn+H2SO4=ZnSO4+H2↑ B>A>C
本题解析:A中铁与稀H2SO4反应;B中形成Sn-H2SO4-Fe原电池,其中Fe作负极,Sn作正极,负极的电极反应是Fe—2e-=Fe2+,正极的电极反应是2H++2e-=H2↑;C中形成Zn-H2SO4-Fe原电池,Zn作负极被腐蚀,总反应方程式为Zn+H2SO4=ZnSO4+H2↑。比较A、B、C三种情况可知:B中Fe作负极,被腐蚀得最快,C中的Fe作正极,被腐蚀得最慢。
本题难度:简单
2、选择题 关于下图所示装置的说法中,不正确的是
A.锌片是该装置的负极,该电极反应为Zn—2e—=Zn2+
B.电子由锌片通过导线流向铜片
C.该装置能将化学能转化为电能
D.铜片上发生氧化反应
参考答案:D
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,铜是正极,因此选项D不正确,答案选D。
本题难度:一般
3、选择题 把a?b?c?d四块金属片浸入稀硫酸中,用导线两两相连组成原电池?若a?b相连时,a为负极;c?d相连时,电流由d到c;a?c相连时,c极上产生大量气泡;b?d相连时,b上产生大量气泡?则四种金属的活动性顺序由强到弱的是
A.a>b>c>d
B.a>c>d>b
C.c>a>b>d
D.b>d>c>a
参考答案:B
本题解析:
a、b相连时,a为负极,活泼金属作负极,所以a的金属活动性大于b;
c、d相连时,电流由d到c,电流由正极流向负极,所以c作负极d作正极,c的金属活动性大于d;
a、c相连时,c极上产生大量气泡,c上得电子发生还原反应,所以a上失电子发生氧化反应,故a的金属活动性大于c;
b、d相连时,b上产生大量气泡,所以d是负极,b是正极,d的金属活动性大于b;
所以a、b、c、d4块金属的活动性由强到弱的顺序为a>c>d>b。
考点:考查原电池的工作原理
点评:本题考查了原电池的工作原理,负正极的反应类型及反应特点,难度不大。解题的关键是理解并记熟两极反应的特点及反应类型。
本题难度:一般
4、选择题 在原电池和电解池的电极上所发生的反应,属于氧化反应的是
[ ? ]
A.原电池的正极和电解池的阳极所发生的反应
B.原电池的正极和电解池的阴极所发生的反应
C.原电池的负极和电解池的阳极所发生的反应
D.原电池的负极和电解池的阴极所发生的反应
参考答案:C
本题解析:
本题难度:简单
5、填空题 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa、25℃时,16g
N2H4在氧气中完全燃烧生成氮气,放出热量312 kJ。N2H4完全燃烧反应的热化学方程式是____________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:正极的电极反应式是________________。负极的电极反应式是__________________。
(3)下图是一个电化学过程示意图。 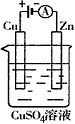
① 锌片上发生的电极反应是______________________。
② 假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼-空气燃料电池理论上消耗标准状况下的空气___________L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是___________________________。
参考答案:“略”
本题解析:
本题难度:一般