时间:2017-08-06 10:40:53
1、选择题 下列有关铝土矿中提炼铝的说法不正确的是
A.铝土矿中的铝元素是以化合态存在的,需用化学方法把铝元素变成游离态
B.提炼过程中,先将铝土矿净化提取氧化铝,再进行冶炼
C.可用常见的还原剂把氧化铝中的铝还原出来
D.冶炼铝的方法同工业冶炼钠、镁相似, 可用电解法
参考答案:C
本题解析:A 正确,铝土矿中铝以氧化铝的形式存在,需用化学方法把铝元素变成游离态
B 正确,先提纯氧化铝。
C 错误,应该用电解熔融的氧化铝的反应冶炼铝。
D 正确,钠、镁、铝都是活泼金属,都用电解法冶炼。
本题难度:一般
2、选择题 下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是
①NaHCO3?②Al2O3?③Al(OH)3?④Al
A.③④
B.②③④
C.①③④
D.全部
参考答案:D
本题解析:能与酸反应又能与碱反应的物质有:弱酸铵盐、弱酸酸式盐、氨基酸、蛋白质、酯、铝、氧化铝、氢氧化铝等;
本题难度:一般
3、选择题 工业利用冶铜炉渣(含Fe2O3、FeO、SiO2、Al2O3等)制Fe2O3的生产流程示意图如下:
经“足量的NaOH溶液”处理后,铝元素的存在形态为(?)
A.Al
B.Al(OH)3
C.Al3+
D.[Al(OH)4]-
参考答案:D
本题解析:足量的NaOH溶液,铝元素的存在形态为[Al(OH)4]-,Al3+ +4OH-=AlO2-+2H2O;
本题难度:一般
4、计算题 (15分)某同学对“铝 热反应”的现象有这样的描述:“反应放出大量的热,并放出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入沙中”。由化学手册查阅得有关物质的熔、沸点数据如下表。
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | ? |
参考答案:Ⅰ.(1)合理(1分)
(2)NaOH溶液(2分) 2Al+2OH-+2H2O===2AlO+3H2↑(2分)
Ⅱ.(1) H++OH-===H2O(2分)
(2)NH+OH-===NH3・H2O或NH+OH-===NH3↑+H2O(2分)
(3)H+ > Fe3+ > Al3+ > NH(2分)
(4)0.008(2分)
(5)0.032(1分),7(1分)
本题解析:铝热反应2Al+Fe2O3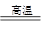 2Fe+Al2O3?2Al+2OH-+2H2O===2AlO+3H2↑
2Fe+Al2O3?2Al+2OH-+2H2O===2AlO+3H2↑
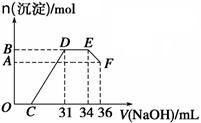
依图可知OC段酸碱中和,加入31ml的碱产生铝和铁的沉淀,34---36ml生成的氢氧化铝被强碱溶解。
Al(OH)3+OH-=AlO+2H2O
4 mol・L-1×4ml
本题难度:一般
5、选择题 一定量的铁铝合金与300 mL 2 mol/L HNO3完全反应生成3.36 L NO(S・T・P)和三价铁盐、铝盐等,再向反应后的溶液中加入3 mol/L NaOH溶液,使铁、铝元素完全沉淀下来,则所加入溶液的体积是(?)
A.150 mL
B.200 mL
C.450 mL
D.无法计算
参考答案:A
本题解析:
硝酸的物质的量为:0.3L×2mol・L-1=0.6mol,生成NO的物质的量为: 3.36L/22.4L・mol-1=0.15mol,所以反应后溶液中NO3-离子的物质的量为0.6mol-0.15mol=0.45mol,再向反应后的溶液中加入 3mol・L-1的NaOH 溶液,使铝镁铁元素恰好全部转化为沉淀,则反应后溶液的成分为NaNO3,所以n(NaOH)=n(NO3-)=0.45mol,则所加 NaOH 溶液的体积是V=n/c=0.45mol/3mol・L-1=0.15L,即150ml.
选A.
本题难度:一般