时间:2017-08-06 10:40:53
1、填空题 现有等物质的量的Mg和Al的混合物a g与100 ml盐酸反应,(气体体积均以标准状况计算)
(1)、该混合物中Mg和Al的质量比为?
(2)、如果金属与盐酸恰好完全反应,则盐酸的浓度为?
(3)、如果反应后金属有剩余,盐酸不足,要计算生成H2的体积,还需要知道?
2、填空题 盐R的化学式为XmYbZp(X、Y、Z为三种不同离子),其组成元素均为短周期元素,取两份等质量等浓度R的水溶液各5 mL进行如下实验:
I.取一份R的水溶液与过量的Ba(OH)2溶液反应,反应过程中生成白色沉淀,沉淀量先增加后减少,最终剩余沉淀甲2.33 g,且甲不溶于稀盐酸。
Ⅱ.取另一份R的水溶液与过量的NaOH溶液混合加热,生成具有刺激性气味的气体乙0.112 L(标准状况),乙能使湿润的红色石蕊试纸变蓝。
据此回答:
(1)写出R和甲的化学式:R___,甲____。
(2)另取1 LR的水溶液,向其中逐滴加入NaOH溶液,所得沉淀与加入NaOH的物质的量关系如图所示。则: 
①R溶液的物质的量浓度为____。
②BC段表示的含义是____。
③CD段反应的离子方程式为____。
3、选择题 14g铜、银合金与足量的某浓度的硝酸反应,将放出的气体与1.12L(标准状况下)氧气混合,通入水中恰好全部被吸收,则合金中铜的质量为 (? )
A.9.6g
B.6.4g
C.3.2g
D.1.6g
4、简答题 将0.1mol镁、铝合金溶于100mL2mol/L的H2SO4溶液中,然后滴加1mol/L的NaOH溶液,生成沉淀与所加NaOH溶液体积的关系如图所示.试回答下列问题:
(1)当溶液中Mg2+、Al3+恰好沉淀完全时,V(NaOH)=______mL;
(2)当V1=160mL时,金属粉末中镁的物质的量为多少?此时V2的值又是多少?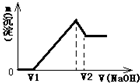
5、选择题 甲、乙两烧杯中分别盛有10mL?1mol?L-1AlCl3溶液,在甲烧杯中加入一定量NaOH溶液;乙烧杯中加入与上述NaOH溶液等体积、等pH的氨水.下列有关两个烧杯的说法中,正确的是
A.甲中产生的沉淀一定比乙中多
B.乙中产生的沉淀一定比甲中多
C.甲和乙产生的沉淀一定一样多
D.甲和乙中产生的沉淀可能一样多