时间:2017-08-06 09:22:43
1、选择题 如图所示的装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色。下列说法中正确的是( )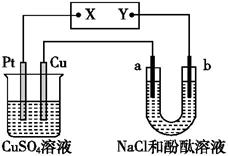
A.X是负极,Y是正极
B.Pt是阴极,Cu是阳极
C.CuSO4溶液的酸性逐渐增强
D.CuSO4溶液的酸性不变
参考答案:C
本题解析:通电一段时间后,b电极附近溶液呈红色,这说明b电极周围溶液显碱性,从b电极是阴极,则Y是负极,X是正极,Pt是阳极,溶液中的OH-放电生成氧气。铜电极是阴极,铜离子放电析出铜,同时还有硫酸生成,所以选项A、B、D都是错误的,正确的答案选C。
本题难度:一般
2、选择题 将含有0.4mo l Cu(N03)2和0.3 mol KCl 的水溶液 1 L,用惰性电极电解一段时间后,在一个电极上析出 0.1 mol Cu ,此时要将溶液恢复到电解前溶液一样,可加入一定量的
l Cu(N03)2和0.3 mol KCl 的水溶液 1 L,用惰性电极电解一段时间后,在一个电极上析出 0.1 mol Cu ,此时要将溶液恢复到电解前溶液一样,可加入一定量的
A.CuCl2
B.CuO
C.Cu(OH)2
D.CuCO3
参考答案:A
本题解析:略
本题难度:一般
3、选择题 下列有关说法中正确的是
A.合成氨中采用及时分离氨气提高反应物的转化率
B.升高温度能使吸热反应速率加快,使放热反应速率减慢
C.增大压强,化学反应速率一定加快,平衡一定发生移动
D.工业上电解饱和食盐水的阴极反应:2Cl--2e-===Cl2↑
参考答案:A
本题解析:A、分离生成物,可使平衡向正向移动,可提高反应物的转化率,A正确;B、升高温度,无论是吸热反应还是放热反应,反应速率都增大,B错误;C、压强只适用于气体,如是固体或纯液体,则增大压强,反应速率不变,平衡不移动,且如为气体,反应物与生成物计量数之和相等,则改变压强,平衡也不移动,C错误;D、阴极发生还原反应,应生成氢气,D错误答案选A。
考点:考查化学平衡的影响因素。
本题难度:一般
4、计算题 以石墨为电极,电解1L硫酸铜和氯化钠的混合溶液,其中硫酸铜与氯化钠的物质的量之和为0.2mol,硫酸铜的物质的量占总物质的量的比值为x。
(1)若x=0.5,当Cu2+在阴极恰好全部析出时,阳极产生的气体是什么?其物质的量是多少?所得溶液的pH是多少?
⑵电解一段时间后,阴、阳两极产生气体的物质的量恰好相等,均为0.16mol,求此时x的值
参考答案:Cl2? 0.05mol? O2? 0.025 mol? 1? 0.6
本题解析:(1)若x=0.5,则硫酸铜是0.1mol,氯化钠是0.1mol。阴极首先是铜离子放电,Cu2++2e-=Cu,所以当铜离子放电完毕之后,转移的电子是0.2mol。在阳极上先是氯离子放电,2Cl--2e-=Cl2↑。氯化钠是0.1mol,生成氯气0.05mol,转移电子是0.1mol,所以根据得失电子守恒可知,在阳极上还有氧气生成。因为4OH--4e-=2H2O+O2↑,所以氧气是 。则同时产生的氢离子是0.1mol,浓度为0.1mol/L,pH是1.
。则同时产生的氢离子是0.1mol,浓度为0.1mol/L,pH是1.
(2)阴、阳两极均产生气体,说明在阴极上当铜离子放电完毕之后,溶液中的氢离子开始放电,2H++2e-=H2↑,氢气是0.16mol,得到电子0.32mol。原混合液中氯化钠最多是0.2mol,即氯离子最多失去0.2mol电子,所以阳极一定还有氧气生成。硫酸铜是0.2xmol,需要得到电子0.4xmol。氯化钠是0.2(1-x)mol。生成氯气是0.1(1-x)mol,则氧气的物质的量是0.16mol-0.1(1-x)mol=(0.06mol+0.1xmol)。根据得失电子守恒可知0.32mol+0.4xmol=0.2(1-x)mol+4×(0.06mol+0.1xmol),解得x=0.6.
本题难度:一般
5、选择题 在某电解质溶液里,用M和N作电极,通电一段时间后,发现M极质量减小,N极质量增大,符合这一情况的是(?)
A.电解质溶液是稀硫酸
B.金属M是阳极,金属N是阴极
C.M和N都是石墨电极
D.M是阴极,N是阳极
参考答案:B
本题解析:通电一段时间后,发现M极质量减小,N极质量增大,这说明M电极是阳极,N电极是阴极,溶液中的金属阳离子得到电子而析出,所以符合条件的是B,答案选B。
点评:在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所据此可以进行有关判断。
本题难度:一般