时间:2017-08-01 02:29:12
1、选择题 下列对分子或离子的立体构型判断不正确的是? ( )。
A.NH4+和CH4都是正四面体形
B.CO2和CS2都是直线形
C.NCl3和BCl3都是三角锥形
D.H2O和H2S都是V形
参考答案:C
本题解析:NCl3是三角锥形分子,BCl3是平面三角形分子。
本题难度:简单
2、填空题 (15分)砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩.
(1)基态砷原子的电子排布式为_______________,砷与溴的第一电离能较大的是______.
(2)AsH3是无色稍有大蒜味气体.AsH3的沸点高于PH3,其主要原因是
________________________________________________.
(3)Na3AsO4可作杀虫剂.AsO43-的空间构型为_____________,与其互为
等电子体的一种分子为______________.
(4)某砷的氧化物俗称“砒霜”,其分子结构如图所示,该化合物的分子式为__________,As原子采取_______杂化.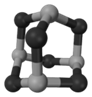
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与_______个Ga相连,As与Ga之间存在的化学键有_____________(填字母)。
A.离子键
B.氢键
C.配位键
D.金属键 E.极性键
参考答案:(1)[Ar]3d104s24p3(2分)? Br(或溴)(1分)
(2)AsH3的相对分子质量大于PH3的相对分子质量,故AsH3分子间作用力大于PH3分子间作用力(2分)
(3)正四面体形(2分)? CCl4(或其他合理答案)(1分)
(4)As4O6(2分)? sp3(2分)?(5)4(1分)? C E(2分)
本题解析:(1)根据构造原理可知,基态砷原子的电子排布式为[Ar]3d104s24p3。非金属性越强,第一电离能越大,所以溴的第一电离能大于砷的。
(2).AsH3和PH3形成晶体都是分子晶体,其沸点高低与分子间作用力强弱有关系。由于AsH3的相对分子质量大于PH3的相对分子质量,故AsH3分子间作用力大于PH3分子间作用力,所以AsH3的沸点高于PH3的。
(3)根据AsO43-的结构可知,其空间构型是正四面体。等电子体是指价电子数和原子数分别都相等的物质。AsO43-中价电子数是5+6×4+3=32,所以与其互为等电子体的是四氯化碳。
(4)根据砒霜的分子结构图可知,分子式为As4O6,由于化学键都是单键,所以是sp3杂化。
(5)晶体结构与金刚石相似,所以GaAs晶体中,每个As与4个Ga相连。As与Ga之间存在的化学键是极性键,由于Ga的价电子是3个,所以还存在配位键,答案选CE。
本题难度:一般
3、选择题 下列物质中不含共价键的是
[? ]
A.NH4Cl
B.NaOH
C.KBr
D.Na2O2
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列物质的分子中既有σ键,又有π键的是
[? ]
①HCl②H2O③N2④H2O2⑤C2H4⑥C2H2
A.①②③
B.③④⑤⑥
C.①③⑥
D.③⑤⑥
参考答案:D
本题解析:
本题难度:简单
5、选择题 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中?T?所处的周期序数与族序数相等.下列判断不正确的是( )
A.最简单气态氢化物的热稳定性:R>Q
B.最高价氧化物对应水化物的酸性:Q<W
C.原子半径:T>Q>R
D.含?T?的盐溶液一定显酸性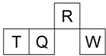
参考答案:D
本题解析:
本题难度:一般