时间:2017-08-01 01:56:35
1、选择题 下列关于0.10 mol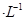 NaHSO3溶液的说法正确的是
NaHSO3溶液的说法正确的是
A.加入NaOH固体,溶液pH减小
B.温度升高,c(HSO3-)增大
C.25 C时,加水稀释后,n(H+)与n(OH-)的乘积变大
C时,加水稀释后,n(H+)与n(OH-)的乘积变大
D.NaHSO3的电离方程式为NaHSO3 = Na++H++SO32-
参考答案:C
本题解析:根据NaHSO3+NaOH=Na2SO3+H2O,加入NaOH固体,溶液PH增大,A项错误;HSO3-的电离过程和水解过程都是吸热过程,温度升高,电离过程增大,水解程度增大,c(HSO3-)减小,B项错误;在同一溶液中,n(H+)?n(OH-)=C(H+)?c(OH-)V×V=KwV×V,加水稀释,KW不变,V增大,则加水稀释后,n(H+)与n(OH-)的乘积变大,C项正确;钠盐是强电解质,电离方程式为NaHSO3 = Na++HSO3-,D项错误;选C。
考点:考查NaHSO3溶液中各种关系。
本题难度:一般
2、选择题 高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数 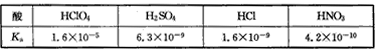
从以上表格中判断下列说法正确的是?
[? ]
A.在冰醋酸中这四种酸都没有完全电离
B.在冰醋酸中高氯酸是这四种酸中最弱的酸
C.在冰醋酸中硫酸的电离方程式为H2SO4==2H++SO42-
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
参考答案:AD
本题解析:
本题难度:一般
3、选择题 下列图示与对应的叙述相符的是



图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
A.图Ⅰ表示t℃时冰醋酸在稀释过程中溶液导电性的变化
B.图Ⅱ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图Ⅲ表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的大
3C(g)+D(s)的影响,乙的压强比甲的大
D.据图Ⅳ,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右
参考答案:D
本题解析:A中,冰醋酸的导电性应该为0,所以A错误;B中,表示的应该为放热反应分别在有、无催化剂的情况下反应过程中的能量变化,不是吸热,所以B错误;C中错在乙的压强比甲的大,因为对可逆反应2A(g)+2B(g) 3C(g)+D(s),压强越大,反应物的百分比就越小,但是最终的百分比并不相等,故C错误;D项则是正确选项
3C(g)+D(s),压强越大,反应物的百分比就越小,但是最终的百分比并不相等,故C错误;D项则是正确选项
考点:化学平衡,电解质的导电,离子水解
点评:该题具有一定的综合性,并且还结合了图像,是高考考查的重点,具有一定的难度。
本题难度:困难
4、选择题 对室温下100 mL pH=2的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
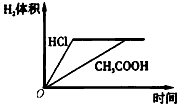
[? ]
参考答案:B
本题解析:
本题难度:一般
5、选择题 证明氨水是弱碱的事实是(?)
A.氨水与硫酸发生中和反应
B.氨水能使紫色石蕊液变蓝
C.0.1 mol/L的NH4Cl溶液的pH值为5.1
D.铵盐与熟石灰反应逸出氨气
参考答案:C
本题解析:略
本题难度:简单