时间:2017-08-01 01:54:23
1、选择题 向水中加入等物质的量Ag+、Na+、Pb2+、Cl-、SO42-、NO3-,用惰性电极电解所得溶液,一段时间后氧化产物与还原产物物质的量之比为
A.8∶1
B.2∶1
C.1∶1
D.1∶2
参考答案:D
本题解析:向水中加入等物质的量的Ag+、Na+、Pb2+、Cl-、SO42-、NO3-,发生反应Ag++Cl-=AgCl↓、Pb2++SO42-=PbSO4 ↓,所以混合溶液中只有Na+、NO3-,电解该溶液,实际上是电解水,则一段时间后氧化产物(氧气)与还原产物(氢气)物质的量之比为 1:2,选 D。
考点:考查电解的计算。
本题难度:一般
2、选择题 下列有关离子方程式与所述事实相符且正确的是
A.用惰性电极电解CuCl2溶液2Cu2+2H2O 4H++O2↑+2Cu
4H++O2↑+2Cu
B.Ba(OH)2溶液中滴加NaHSO4溶液至中性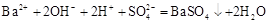
C.漂白粉溶液在空气中失效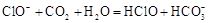
D.用氯化铁溶液和沸水反应制取氢氧化铁胶体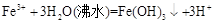
参考答案:B
本题解析:A.用惰性电极电解CuCl2溶液,在阳极Cl-放电,在阴极Cu2+放电,电解池总反应为Cu2++2Cl-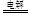 Cl2↑+Cu,A项错误; B.Ba(OH)2溶液中滴加NaHSO4溶液至中性Ba2++2OH-+2H++SO42-=BaSO4 ↓+2H2O,B项正确;C.漂白粉溶液在空气中失效是因为Ca2++2ClO-+CO2 +H2O =2HClO+CaCO3 ↓,2HClO
Cl2↑+Cu,A项错误; B.Ba(OH)2溶液中滴加NaHSO4溶液至中性Ba2++2OH-+2H++SO42-=BaSO4 ↓+2H2O,B项正确;C.漂白粉溶液在空气中失效是因为Ca2++2ClO-+CO2 +H2O =2HClO+CaCO3 ↓,2HClO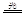 2HCl+O2↑,C项错误;D.用氯化铁溶液和沸水反应制取的氢氧化铁胶体是红褐色溶液,不是沉淀,D项错误;选B。
2HCl+O2↑,C项错误;D.用氯化铁溶液和沸水反应制取的氢氧化铁胶体是红褐色溶液,不是沉淀,D项错误;选B。
考点:考查离子方程式的正误判断。
本题难度:困难
3、选择题 如图所示,下列叙述正确的是
[? ]
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X与滤纸接触处变红
参考答案:A
本题解析:
本题难度:一般
4、选择题 下图为直流电源电解稀Na2SO4溶液的装置。通电一段时间后,在石墨电极a和b附近分别滴加一滴酚酞溶液。则下列有关说法中正确的是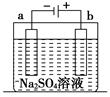
A.a电极产生H2
B.两极产生的气体均有刺激性气味
C.通电一段时间后,稀Na2SO4溶液酸性增强
D.a电极附近呈无色,b电极附近呈红色
参考答案:A
本题解析:惰性电极电解硫酸钠溶液,相当于电解水,阴极氢离子放电生成氢气,阳极OH-放电生成氧气,所以阴极周围溶液显碱性,阳极周围溶液显酸性,A.a是阴极,产生氢气,正确;B.阴极生成氢气,阳极生成氧气,均是无色无味气体,错误;C. 惰性电极电解硫酸钠溶液,相当于电解水,通电一段时间后,稀Na2SO4溶液仍呈中性,错误;D. a电极附近呈红色,b电极附近呈无色,错误;选A。
考点:考查电解池。
本题难度:一般
5、计算题 某氯碱厂日产50% NaOH溶液3000 kg。
(1)试计算该厂每天生产Cl2和H2的体积(标准状况)。
(2)如果把这些Cl2和H2都制成38%的盐酸,试计算理论上每天可生产盐酸的质量。
参考答案:(1)4.2×105 L? 4.2×105 L
(2)3601.97 kg
本题解析:(1)设该厂每天生产Cl2和H2的体积为x、y,有
2NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
2×40 g? 22.4 L 22.4 L
3000×103 g×50%?x? y
x=y=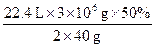 =
=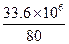 =4.2×105 L
=4.2×105 L
(2)设理论上每天能生产38%的盐酸的质量为z,有
z=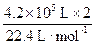 ÷38%="3601973.6" g="3601.97" kg
÷38%="3601973.6" g="3601.97" kg
另解:由关系式得:NaOH? ~? HCl
40? 36.5
3000×50%?E・38%
E="3601.97" kg
本题难度:简单