时间:2017-08-01 01:42:49
1、填空题 在H2S溶液中,通入或加入少量下列物质:①O2?②Cl2?③SO2?④CuSO4,能使溶液中的c(H+)增大的是______________。
参考答案:②④
本题解析:H2S是弱电解质,在溶液中存在如下平衡:H2S H++HS-,HS-
H++HS-,HS- H++S2-。当加入少量CuSO4时,Cu2+会与S2-结合成难溶于酸的沉淀,使c(S2-)减小,使上述平衡向右移动,导致溶液中c(H+)增大。若通入O2、Cl2、SO2气体,它们都能与H2S反应。O2与H2S反应生成S和H2O,c(H+)下降。SO2与H2S反应生成S和H2O,但题目中说明“少量”,故不应考虑SO2过量。Cl2与H2S反应生成S和HCl,使c(H+)增大。
H++S2-。当加入少量CuSO4时,Cu2+会与S2-结合成难溶于酸的沉淀,使c(S2-)减小,使上述平衡向右移动,导致溶液中c(H+)增大。若通入O2、Cl2、SO2气体,它们都能与H2S反应。O2与H2S反应生成S和H2O,c(H+)下降。SO2与H2S反应生成S和H2O,但题目中说明“少量”,故不应考虑SO2过量。Cl2与H2S反应生成S和HCl,使c(H+)增大。
本题难度:简单
2、选择题 下列物质最难电离出H+的是( )
A.CH3COOH
B.C2H5OH
C.H2O
D.H2CO3
参考答案:B
本题解析:
本题难度:简单
3、选择题 将0.1mol?L-1的醋酸钠溶液20mL与0.1mol?L-1的盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
A.c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH)
B.c(CH3COO-)>c(H+)>c(CH3COOH)>c(Cl-)
C.c(CH3COO-)=c(Cl-)>c(H+)>c(CH3COOH)
D.c(Na+)+c(H+)=c(CH3COO-)+c(Cl-)+c(OH-)
参考答案:将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后,反应后NaAc和HAc的物质的量相等,溶液显酸性,说明HAc电离程度大于Ac-水解程度,
A.HAc为弱电解质,部分电离,应有c(HAc)>c(H+),故A错误;
B.反应后NaAc和HAc的物质的量相等,溶液显酸性,说明HAc电离程度大于Ac-水解程度,则(Ac-)>c (Cl-),HAc为弱电解质,部分电离,应有c(HAc)>c(H+),故B错误.
C.反应后NaAc和HAc的物质的量相等,溶液显酸性,说明HAc电离程度大于Ac-水解程度,则(Ac-)>c (Cl-),故C错误;
D.溶液遵循电中性原则,应有c(Na+)+c(H+)=c(Ac-)+c(Cl-)+c(OH-),故D正确.
故选D.
本题解析:
本题难度:简单
4、选择题 醋酸溶液中存在电离平衡:CH3COOH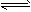 H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
[? ]
A.CH3COOH溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B.0.1 mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)减小
C.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动
D.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
参考答案:B
本题解析:
本题难度:一般
5、选择题 一定温度下,向0.1 mol・L-1 CH3COOH溶液中加少量水,下列有关说法错误的是(?)
A.溶液中所有离子的浓度都减小
B.CH3COOH的电离程度变大
C.水的电离程度变大
D.溶液的pH增大
参考答案:A
本题解析:A选项错误,H+浓度减小,OH-浓度增大;B选项正确,溶液越稀,弱电解质的电离程度越大;C选项正确,酸溶液中OH-主要是由水电离产生的,OH-浓度变大,说明水的电离程度变大;D选项正确,由于H+浓度减小,故溶液的pH增大。
本题难度:一般