时间:2017-08-01 01:34:50
1、选择题 如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
A.蓝色石蕊试纸先变红后褪色
B.NaOH溶液可用于除去实验中多余的SO2
C.湿润淀粉KI试纸未变蓝说明SO2的氧化性弱于I2
D.品红试纸、沾有KMnO4溶液滤纸均褪色都能证明SO2的漂白性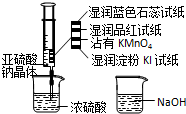
参考答案:BC
本题解析:
本题难度:一般
2、简答题 为了探究硫化钠晶体(Na2S?nH2O)在空气中的变化,某兴趣小组的实验步骤及现象记录如下:①将少量硫化钠晶体置于表面皿上,暴露在空气中;②三天后将样品放入盛水的烧杯中,搅拌后得无色澄清溶液;③取少量该溶液加入过量盐酸中,有气体放出,且溶液保持澄清.
(1)请你根据上述记录,对放出气体进行猜想:
猜想①:可能是H2S;?猜想②:可能是SO2;?猜想③可能是CO2;
猜想④:可能是______;?猜想⑤:可能是______.
(2)若放出的气体是两种气体的混合气,现有:浓、稀2种品红溶液,浓、稀2种溴水,澄清石灰水,浓、稀2种盐酸溶液、试管气体发生装置,洗气瓶、试管洗气装置.请设计一个组合实验分析混合气的组成,在下表中简要写出实验方法、现象和结论:
| 实验方案 | 可能的现象和相应的结论 |
| ______ ______ ______ |
参考答案:(1)因硫化钠变质后产物可能为Na2SO3、Na2SO4、Na2CO3,Na2S、Na2SO3、Na2SO4、Na2CO3之间不反应,Na2S、Na2SO3、Na2CO3与盐酸反应分别得到H2S、SO2、CO2,Na2SO4与盐酸不反应,产生的气体可以是单一气体,也可以是混合气体,但混合气体不能为SO2与H2S,因为两者反应生成硫沉淀,所以混合气体可以为H2S与CO2的混合气,也可以为SO2和CO2的混合气体,故答案为:H2S与CO2的混合气体;SO2?和CO2的混合气体;
(2)先通过浓溴水一方面可观察H2S被氧化生成S沉淀现象,另一方面可尽量吸收氧化SO2,以防SO2进入后一步澄清石灰水溶解CaCO3而干扰观察;在石灰水前面加装稀溴水洗气装置是为了便于观察SO2是否在上一步吸收完全,选稀品红溶液易观察褪色现象,故答案为:
实验方案可能的现象和相应的结论在试管气体发生装置中加入适量的固体样品和稀盐酸,组装好后将产生体依次通过盛有稀品红溶液、浓溴水、稀溴水和澄清石灰水的试管洗气装置.若品红褪色,溴水颜色变浅不浑浊,澄清石灰水变浑浊,该气体含有SO2、CO2的混合气体若品红不褪色,溴水褪色(或变浅)且有浑浊出现,澄清石灰水变浑浊,该气体为H2S、CO2的混合气体(3)因硫酸根离子的检验方法:滴加BaCl2溶液,若有沉淀出现说明有硫酸根离子,故答案为:取题中实验③后所得溶液滴入BaCl2溶液,若有沉淀出现说明生成了Na2SO4;若无沉淀,则说明没有生成Na2SO4.
本题解析:
本题难度:一般
3、选择题 既能使石蕊试液变红,又能使品红试液变为无色的物质是( )
A.NH3
B.HCl
C.SO2
D.CO2
参考答案:A、氨气既不能使石蕊试液变红,又不能使品红试液变为无色,故A错误;
B、氯化氢能使石蕊试液变红,但是不能使品红试液变为无色,故B错误;
C、二氧化硫具有漂白性,溶于水溶液酸性酸性,既能使石蕊试液变红,又能使品红试液变为无色,故C正确;
D、二氧化碳没有漂白性,不能够使品红试液变为无色,故D错误;
故选C.
本题解析:
本题难度:一般
4、选择题 某气体通入品红溶液中,品红溶液褪色,再加热时恢复为原来的颜色,该气体是( )
A.N2
B.SO2
C.CO2
D.H2
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列关于SO2性质的说法中,不正确的是
[? ]
A.能与水反应生成硫酸
B.能使品红溶液褪色
C.能与NaOH溶液反应
D.能使酸性KMnO4溶液褪色
参考答案:A
本题解析:
本题难度:简单