时间:2017-08-01 01:33:44
1、填空题 甲、乙、丙三种物质之间有如下转化关系: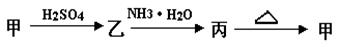
(1)若甲是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是_______ 。写出乙 丙转化的离子方程式 :________________________ 。
丙转化的离子方程式 :________________________ 。
(2)若乙溶液中加入KSCN溶液 ,有血红色出现,则甲物质是__________,乙物质的水溶液显?性(“酸”或“碱”),原因是?(用离子方程式表示)。
参考答案:
本题解析:(1)Al2O3? Al3++3NH3·H2O =Al(OH)3↓+3NH4+
(2)Fe2O3? Fe3++3H2O Fe(OH)3+3H+ (1)若甲是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,且丙加热生成甲,则甲是氧化铝,丙是氢氧化铝,乙是硫酸铝,则乙
Fe(OH)3+3H+ (1)若甲是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,且丙加热生成甲,则甲是氧化铝,丙是氢氧化铝,乙是硫酸铝,则乙 丙转化的离子方程式是Al3++3NH3·H2O =Al(OH)3↓+3NH4+。
丙转化的离子方程式是Al3++3NH3·H2O =Al(OH)3↓+3NH4+。
(2)若乙溶液中加入KSCN溶液 ,有血红色出现,这说明乙中含有铁离子,所以丙是氢氧化铁,则甲是氧化铁,因此乙是硫酸铁。在溶液中铁离子水解,溶液显酸性,反应的离子方程式是Fe3++3H2O Fe(OH)3+3H+。
Fe(OH)3+3H+。
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。
本题难度:一般
2、实验题 (6分)某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。回答下列问题: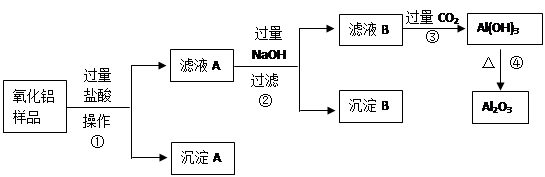
(1)操作①的名称?;
(2)沉淀A的化学式是___________,滤液B中的阴离子除了Cl—、OH—外还有______________;
(3)步骤④的化学方程式为______________________________________;
(4)在操作②中要用到的玻璃仪器除了烧杯、玻璃棒,还有_________________。
参考答案:(1)过虑?(2)SiO2? AlO2-?(3)2Al(OH)3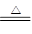 ?Al2O3 + 3H2O?(4)普通漏斗
?Al2O3 + 3H2O?(4)普通漏斗
本题解析:二氧化硅不溶于盐酸,通过过滤即得到沉淀A。滤液中含有的是过量的盐酸,生成的氯化铁和氯化铝。加入过量的氢氧化钠溶液后氯化铁生成氢氧化铁沉淀,氯化铝生成偏铝酸钠,过滤即得到氢氧化铁沉淀。此时滤液中含有过滤的氢氧化钠和生成偏铝酸钠以及氯化钠,通入过量的二氧化碳即可以生成氢氧化铝沉淀。氢氧化铝不稳定,加热分解生成氧化铝。
本题难度:一般
3、选择题 用稀硫酸,氢氧化钠,铝为原料制取Al(OH)3可通过不同的途径
要制得等量的Al(OH)3,三种不同的途径分别消耗硫酸的比值为
A、12:4:3?B 、3:2:1
、3:2:1
C、9:8:6?D、8:4:3
参考答案:A
本题解析:略
本题难度:一般
4、选择题 氢氧化铝可作为治疗胃酸过多的内服药,这是利用了氢氧化铝的
[? ]
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列反应中,最终生成沉淀的是(?)
A.向氢氧化钠溶液中滴入硫酸铝溶液至过量
B.向偏铝酸钠溶液中滴入盐酸至过量
C.向氯化铝溶液中滴入氢氧化钠溶液至过量
D.向偏铝酸钠溶液中滴入氢氧化钠溶液至过量
参考答案:A
本题解析:A正确,向氢氧化钠溶液中滴入硫酸铝溶液先无沉淀产生,后才有沉淀;B错,现象为先有沉淀后沉淀溶解;C错,现象为先有沉淀,后沉淀消失;D错,无现象;
本题难度:一般