ʱ��:2017-08-01 01:33:44
1��ѡ���� ��Ba(OH)2��Һ����������Һ�У�ʹSO42-?ȫ��ת����BaSO4��������ʱ��Ԫ�ص���Ҫ������ʽ�ǡ�
[? ]
A��Al3+?
B��Al(OH)3?
C��AlO2-?
D��Al3+��Al(OH)3
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� �Ȼ������ε�ⷨ�����Ȼ���Ϊԭ�ϣ��Լ��������������Ȼ��������MgCl2��KCl��CaCl2��Ϊ����ʽ��е����ȡ���ķ�����
��1���Ȼ������ε�ⷨ��Ҫ���ƴ�������������������Ҫ�ɷ�ΪAl2O3����������Fe2O3��SiO2�����ʣ�Ϊԭ��ͨ������;���ᴿ��������
������д��X��Y�ijɷ�?��??��
����ͼ��ʾ��ʵ�����н��й��ˣ������е���������ֱ���?��?��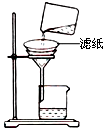
��2���Ʊ���ˮ�Ȼ����ķ�ӦΪ��2Al2O3+6Cl2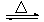 4AlCl3+3O2
4AlCl3+3O2
��Ϊ�ٽ��÷�Ӧ�Ľ��У�ʵ������������뽹̿����ԭ����?��
�ܼ��뽹̿��Ļ�ѧ��Ӧ�ɱ�ʾΪAl2O3+C+Cl2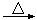 AlCl3+X����Ϊȷ������X�Ƿ��ǻ�����壬ijͬѧ��X����ͨ�����ȵ�����ͭ�ͳ����ʯ��ˮ���ٸ��������жϡ��ò����Ƿ���ȷ��������ȷ������ȷ�����жϣ�?����˵������?��
AlCl3+X����Ϊȷ������X�Ƿ��ǻ�����壬ijͬѧ��X����ͨ�����ȵ�����ͭ�ͳ����ʯ��ˮ���ٸ��������жϡ��ò����Ƿ���ȷ��������ȷ������ȷ�����жϣ�?����˵������?��
��3�����ڹ�ҵ��ͨ���õ��������������ʽ��ȡ��������������1�������ĵ�������������_________
������ڡ�����С�ڡ��������ڡ����Ȼ���������
�ο��𰸣���10�֣���1����NaOH��Һ��1�֣���?ϡ���ᣨ1�֣�
��û��ʹ�ò�������������ֽ��Ե����©����Ե��2�֣�
��2����̼��O2��Ӧ�������ڷ�Ӧ������У�2�֣�
�ܲ���ȷ��������������ͨ�����ȵ�CuO��ĩ������CO�ͻ�����CO2����������ȷ��ԭ���Ƿ���CO2����2�֣�?��3��С�ڣ�2�֣�
�����������1������Һ���ܺͰ�ˮ��Ӧ��������������������˵����Һ���к��������ӣ�����YӦ�������ᡣ����Һ���к���AlO2����SiO32�������X��NaOH�����������������Ʋ���Ӧ�������õ��������������ƺ����ᷴӦ���ɹ�������������õ��Ȼ���������Ļ��Һ�����백����������������������
�ڸ���װ��ͼ��֪����װ���ǹ���װ�ã������Ҫ�Ĵ�������û��ʹ�ò����������������ֽ��Ե����©����Ե��
��2������Ϊ�ڼ��ȵ������£�̼��O2��Ӧ������CO��CO2������������Ũ�ȣ������ڷ�Ӧ������С�
�������ڼ��ȵ������£�CO�ܺ�����ͭ��Ӧ����CO2�����Խ�����������ͨ�����ȵ�CuO��ĩ������CO�ͻ�����CO2����������ȷ��ԭ���Ƿ���CO2�������Dz���ȷ�ġ�
��3������ԭ���غ��֪��1mol��������������2mol�Ȼ�����1mol��������������102g��2mol�Ȼ�����������2mol��133.5g/mol��267g������������������С���Ȼ�����������
�����Ѷȣ�һ��
3��ѡ���� ��100mL 0.6 mol/L�Ȼ�����Һ��1mol/L����������Һ��Ϻõ�3.9g Al(OH)3?��������ʱ��������������Һ�������
A��130mL
B��180mL
C��190mL
D��240mL
�ο��𰸣�C
����������Ȼ��������ʵ�����0.1L��0.6mol/L��0.06mol
�������ɵ�����������������3.9g�����ʵ�����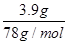 ��0.05mol��0.06mol
��0.05mol��0.06mol
��˵����Ӧ����Ԫ��û����ȫת��Ϊ������������������Ȼ�������������ݷ���ʽ��֪��
Al3��?��? 3OH����Al(OH)3��
1mol? 3mol? 1mol
0.05mol? 0.15mol? 0.05mol
������������������Һ�������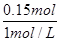 ��0.15L��150ml
��0.15L��150ml
�����Ӧ����Ԫ�ز���ת��ΪAlO2��������ݷ���ʽ��֪
Al3��?��? 3OH����Al(OH)3��
1mol? 3mol? 1mol
0.06mol? 0.18mol? 0.06mol
�����ֱ�����������Һ�ܽ������������0.06mol��0.05mol��0.01mol
Al(OH)3?�� OH����AlO2����2H2O
1mol?1mol
0.01mol? 0.01mol
�����������������Ƶ����ʵ�����0.18mol��0.01mol��0.19mol
�����������������Һ�������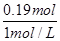 ��0.19L��190ml�����Դ�ѡC��
��0.19L��190ml�����Դ�ѡC��
�����Ѷȣ�һ��
4��ѡ���� 0.1molMg�ֱ���������O2��CO2��N2��ȼ�գ����ɵĹ�����������ΪW1��W2��W3�������й�ϵʽ����ȷ���ǣ�������
A��W2��W1��W3
B��W1=W2��W3
C��W1=W2=W3
D��W3��W2��W1
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5�������� (12��)С�մ�θ��ƽ����ϲ���dz��õ��к�θ���ҩ�
��1��С�մ�ƬÿƬ��0.42 gNaHCO3��2ƬС�մ�Ƭ��θ����ȫ�кͣ����к͵���������
_______mol��
��2��θ��ƽÿƬ��0.135 g Al(OH)3���к�θ��ʱ��6ƬС�մ�Ƭ�൱��θ��ƽ?Ƭ��
��3����ϲ�Ļ�ѧ�ɷ�������þ�ļ�ʽ̼���Ρ�
��ȡ�ü�ʽ̼����2.20g������2.0 mol��L��1����ʹ���ܽ⣬����������30 mLʱ��ʼ����CO2������������35 mLʱ���÷�Ӧ��ȫ������ü�ʽ����Ʒ����������̼��������ʵ���֮��_________��
����������ʽ��������������Һ�м�������������ƣ����ˣ���������и������1.16g�����Ʋ�ü�ʽ�εĻ�ѧʽ_________��
�ο��𰸣�(12��)��1��0.01mol?��2��2?
��3��n(OH��)�Un(CO32��)=5�U1?
��4��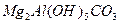
�����������
�����Ѷȣ�һ��