时间:2017-08-01 01:16:19
1、实验题 (15分)某实验小组同学对电化学原理进行了一系列探究活动。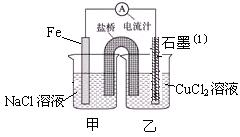
(1)右图为某实验小组依据氧化还原反应:(用离子方程式表示)?设计的原电池装置,一段时间后,两电极质量相差12g,导线中通过?mol电子。
(2)其它条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为?,这是由于NH4Cl溶液显?性,(填酸性、碱性或中性)用离子方程式表示溶液显此性的原因?,用吸管吸出铁片附近溶液少许至于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式?,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式?。
(3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是?,电极反应为?;乙装置中石墨(1)为??极(填正、负、阴、阳),乙装置中与铜线相连石墨电极上发生的反应式为?,产物常用?检验,反应的离子方程式为?。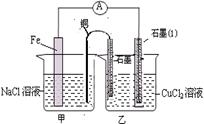
参考答案:
(1)Fe +Cu2+ ="==" Fe2+ + Cu?(1分)? 0.2mol。(1分)
(2)2H+ + 2e-="==" H2↑;酸(各1分)? NH4+ + H2O 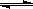 ?NH3・H2O + H+(1分)
?NH3・H2O + H+(1分)
2Fe2+ + Cl2="==" 2Fe3+ + 2Cl-?(1分)?2Fe3++3Cl2+8H2O==2FeO42-?+6Cl-?(2分)
(3)溶液变红(1分)? O2+2H2O+4e―="==" 4OH―(2分)?阴(1分),2Cl――2e―===Cl2↑(1分),
湿润淀粉碘化钾试纸(1分),?Cl2?+ 2I- ="=" 2Cl― ?+I2 (1分)?。
本题解析:略
本题难度:简单
2、选择题 某学生运用所学知识研究钠的性质:将一粒金属钠和一块铜片分别盛在表面皿中,来研究它们在空气中的稳定性。该学生采用的研究方法是
[? ]
①假说法 ②实验法 ③分类法 ④比较法
A.①②
B.①③
C.②④
D.①③
参考答案:C
本题解析:
本题难度:简单
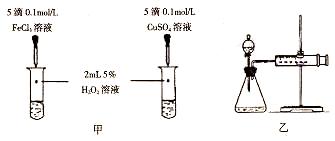
3、实验题 为了研究外界条件对H2O2分解速率的影响,某同学做了以下实验,请回答下列问题。
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5%H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中。 | 试管A中产生气泡量减少;试管B中产生的气泡量增大。 |
| ② | 另取两支试管分别加入5mL 5%H2O2溶液和5mL 10%H2O2溶液 | 试管A、B中均未明显见到有气泡产生。 |
 ?
?
参考答案: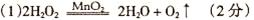
(2)研究温度对H2O2分解速率的影响?(2分)
(3)将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率(2分)
(4)A?(1分)
(5)①溶液中气泡产生的速率?(1分)排除氯离子的干扰(其他合理答案也给分)(1分)
②收集40mL气体所需的时间(1分)(其它合理答案同样给分)
本题解析:考查外界条件对反应速率的影响。
(1)过氧化氢在催化剂的作用下分解生成氧气和水,方程式为2H2O2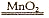 2H2O+O2↑。
2H2O+O2↑。
(2)根据实验过程中的操作可知,目的是研究温度对H2O2分解速率的影响。
(3)用于在实验中没有使用催化剂,且溶液的温度较低,双氧水的分解很慢,所以改进的方法是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率。
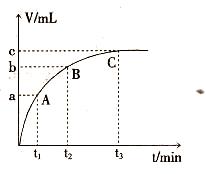
(4)反应速率越快,反映在曲线上的斜率就越大,所以根据图像可知,A点反应速率最快。
(5)①由于反应中产生氧气,所以可通过观察溶液中气泡产生的速率来比较反应快慢。由于两种盐溶液中阴离子特,所以为排除阴离子不同而造成实验的不准确,用硫酸铁最好。
②要想定量分析,则必须测量收集40mL气体所需的时间来比较反应的快慢。
本题难度:简单
4、实验题 (6分)据“网易新闻中心”报道,2008年12月13日,湖北大冶市金牛镇小泉村发生了群体中毒事件,三名儿童在送往医院途中死亡,另两名儿童至今日仍在医院治疗。经诊断,两儿童为灭鼠药“毒鼠强”急性中毒。此前的10月30日,湖北枣阳发生了三十四人的集体毒鼠强中毒事件;而震惊全国的湖北利川“十・二一”毒鼠强投毒案,曾造成三十五人中毒、十人死亡。毒鼠强的毒害是严重的,国家已禁止使用该药来消灭老鼠。那么什么是毒鼠强?它是一种含有C、H、O、N、S的有机物,其摩尔质量为240 g・mol-1,其中所含碳元素的质量分数为20%,所含氢元素的质量分数为3.3%,所含氧元素的质量分数为26.7%,所含氮元素的质量分数为23.3%,所含硫元素的质量分数为26.7%。根据以上各元素在其中所占的质量分数,试求各元素的物质的量之比为______,其化学式为______。
参考答案:n(C)∶n(H)∶n(O)∶n(N)∶n(S)=2∶4∶2∶2∶1 C4H8O4N4S2?
本题解析:根据物质的摩尔质量及各元素的质量分数,可计算出各元素的原子个数及化学式,设该物质1 mol,则质量为240 g。
n(C)==4 mol
n(H)==8 mol
n(O)==4 mol
n(N)==4 mol
n(S)==2 mol
则原子个数比n(C)∶n(H)∶n(O)∶n(N)∶n(S)=4∶8∶4∶4∶2=2∶4∶2∶2∶1。
化学式为C4H8O4N4S2。
本题难度:一般
5、选择题 用如图所示的方法研究某气体的性质,这种方法属于
[? ]
A.分类法
B.观察法
C.实验法
D.比较法
参考答案:B
本题解析:
本题难度:简单