时间:2017-08-01 01:13:46
1、选择题 下列热化学方程式书写及说法正确的是
A.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=" -" 890 kJ
B.C(s)+1/2O2(g)="CO(g)" ΔH=" -" 101.5 kJ·mol-1,该方程式的ΔH可表示碳的燃烧热
C.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) ΔH=" -" 2a kJ·mol-1,则任何强酸和强碱发生中和反应生成1mol H2O(l)的反应热均为-a kJ·mol-1
D.2mol氢气燃烧得水蒸气放热484 kJ,则H2O(g)=H2(g)+1/2O2(g) ΔH=" +" 242 kJ·mol-1
参考答案:D
本题解析:A.热化学方程式中,焓变的单位是kJ·mol-1,错误;B.燃烧热是指1moL物质完全燃烧生成稳定的化合物时放出的热量,碳的稳定生成物是二氧化碳,错误;C.氢氧化钡与硫酸反应生成水外,还有硫酸钡沉淀,所以,任何强酸和强碱发生中和反应生成1mol H2O(l)的反应热不都等于-a kJ·mol-1,错误;D.正确;选D。
考点:考查热化学方程式正误判断。
本题难度:一般
2、选择题 已知大多数含氧酸可用通式XOm(OH)n来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4.一般而言,该式中m大于等于2的是强酸,m为0的是弱酸.下列各含氧酸中酸性最强的是( )
A.H2SeO3
B.HMnO4
C.H3BO3
D.H3PO4
参考答案:A、H2SeO3可以改写为SeO1(OH)2,非羟基氧原子数目为1;
B、HMnO4可以改写为MnO3(OH)1,非羟基氧原子数目为3;
C、H3BO3可以改写为B(OH)3,非羟基氧原子数目为0;
D、H3PO4可以改写为PO1(OH)3,非羟基氧原子数目为1;
HMnO4中非羟基氧原子数目最多,酸性最强.
故选:B.
本题解析:
本题难度:一般
3、选择题 下列叙述错误的是(?)?
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R大于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)H2O、H2S、H2Se的相对分子质量增大,所以熔沸点依次升高
(4)液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
(5)都是由非金属元素形成的化合物只能是共价化合物
A.全部
B.(1)(2)(3)(4)
C.(1)(2)(3)(5)
D.(2)(3)(4)
参考答案:A
本题解析:非金属性越强,最高价氧化物的水化物的酸性越强,因此如果R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R不一定大于Q,(1)不正确;阴、阳离子通过静电作用形成的化学键叫离子键,(2)不正确;水分子间存在氢键,所以在同主族元素的氢化物中沸点最高,(3)不正确;氢键不是化学键,一般影响物质的物理性质,而不能影响物质的稳定性。氢化物的稳定性与化学键有关系冒(4)不正确;都是由非金属元素形成的化合物不一定是共价化合物,也可能是离子化合物,例如氯化铵,(5)不正确,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生分析、归纳和总结问题的能力的培养,有利于调动学生的学习兴趣,激发学生的学习积极性。答题时注意学会排除法,通过举例、逐一筛选得出正确结论的方法。
本题难度:简单
4、选择题 下列说法中正确的是
A.焓变是指1 mol物质参加反应时的能量变化
B.反应放热时,ΔH>0;反应吸热时,ΔH<0
C.在一个确定的化学反应关系中,反应物的总焓与生成物的总焓一定不同
D.在一个确定的化学反应关系中,反应物的总焓总是高于生成物的总焓
参考答案:C
本题解析:
试题解析:在恒温、恒压的条件下,化学化学反应过程中所吸收或释放的热量称为反应的焓变,参加反应的物质的物质的量不一定是1mol,故A错误;放热时体系能量降低,△H<0,吸热时体系能量升高,△H>0,故B错误;任何化学反应过程,一定伴随着能量的变化,反应物的总焓与生成物的总焓一定不同,故C正确;在一个确定的化学反应关系中,当反应物的总焓大于生成物总焓时,反应放出热量,反之吸收热量,故D错误。
考点: 反应热和焓变
本题难度:一般
5、选择题 下列叙述与对应图式正确的是
| | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 主要化合价 | -2 | +2 | +1 | +5、-3 | +7、-1 | +1 | +5、-3 | +3 |
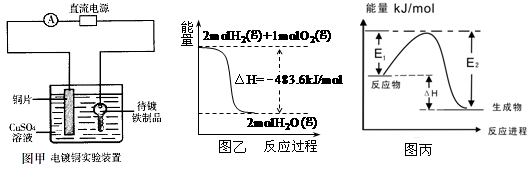
参考答案:B
本题解析:根据表格提供的数据可知:①是O;②是Mg;③是Li;④是P;⑤是F;⑥是Na;⑦是N;⑧是Al。A.由于在上述元素中金属性最强的是Na,所以由下列短周期元素性质的数据推断元素⑥最高价氧化物对应的水化物碱性最强,错误;B.在图甲电镀装置中,待镀铁制品应与电源负极相连,镀层金属与电源的正极连接,作阳极,正确;C.图乙表示H2与O2发生反应过程中的能量变化,由于燃烧热是1mol的可燃物完全燃烧产生稳定的氧化物时所放出的热量,H2O的稳定的氧化性是液态水,则H2的燃烧热的热化学方程式中的△H<— 241.8 kJ/mol ,错误;D.图丙表示某一放热反应,若使用催化剂E1、E2都会发生改变,但是△H不变,错误。
考点:考查元素的性质与原子结构的关系、电镀、热化学方程式的书写及反应热与焓变和活化能的关系的知识。
本题难度:一般