ʱ��:2017-07-31 23:54:18
1������� ��1��H+����H2O�γ�H3O+��H3O+��Oԭ�Ӳ���_______�ӻ�������DZ�ˮ����_______�����С������
��2���������ơ��⡢���ʯ���ɱ����Ȼ��ƾ���ľ���ʾ��ͼ��δ��˳�������������־����о���������ͬ����______________������д��ţ��� 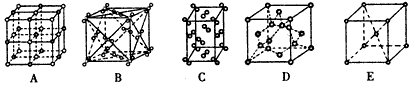
��3���ڱ��ľ����У�ÿ��ˮ���������ڵ�4 ��ˮ�����γ��������ͼ��ʾ������֪���������ȣ���1 mol ˮ�ɱ�ת��Ϊˮ����������������51KJ/mol��������⣬ˮ���Ӽ仹���ڷ��»�����11 kJ/mol �� ���������������ġ����ܡ����ƻ�1mol ��������������Ϊ����ġ����ܡ�����________kJ/mol �� 
��4��CaO��NaCl�ľ���ͬΪ���������ṹ����֪CaO�����ܶ�Ϊag��cm-3����ʾ�����ӵ���������CaO�������Ϊ_______cm3��
��5����������Һ�У�������������ԭ��Ӧ�б������뱻��ԭ�ĵ�Ԫ�ص����ʵ���֮��Ϊ2:5��
��___KBiO3+_____MnSO4+_____H2SO4==_____Bi2(SO4)3+_______+_______+_______
��д��Biͬ�����������Ԫ�صĵ����Ų�ʽ��___________________��
�ο��𰸣���1��sp3����?
��2��BC
��3��20
��4��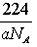
��5����10KBiO3+4MnSO4+14H2SO4==5Bi2(SO4)3+4KMnO4+14H2O+3K2SO4��
��1s22s22p63s23p63d104s24p3
���������
�����Ѷȣ�һ��
2������� ��10�֣���ͭ����Ͻ�����������ʹ�õĽ������ϡ�
����ͼ�ǽ���Ca��Cu���γɵ�ij�ֺϽ�ľ����ṹʾ��ͼ����úϽ���Ca��Cu��ԭ�Ӹ�����Ϊ?��
��Cu2������NH3��H2O��Cl�����γ���λ��Ϊ4������
�٣�Cu(NH3)4��2���д��ڵĻ�ѧ��������?������ţ���
A�����
B��������
C�����Թ��ۼ�
D���Ǽ��Թ��ۼ� E�����Ӽ�
�ڣ�Cu(NH3)4��2�����жԳƵĿռ乹�ͣ���Cu(NH3)4��2���е�����NH3������Cl��ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ�����Cu(NH3)4��2���Ŀռ乹��Ϊ?��
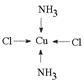
�����������ֲ�ͬ�ṹ�IJ���Ľṹ��ʽ��������λ������
�ο��𰸣��� 1:5 ��?��A��C ��ƽ�������ͣ�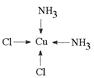 ��
��
�����������1�����ݾ����ṹ��֪���þ����к��е�Ca��8��1/8��1�����е�Cu��8��1/2��1��5������ԭ�Ӹ���֮����1�U5��
��2�����������һ��������λ����A��ȷ�����ⰱ���л����ڼ��Լ������Դ�ѡAC��
�ڣ�Cu(NH3)4��2���е�����NH3������Cl��ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ��˵���ṹ�������������ͣ�����ƽ�������νṹ�����������ʵĽṹ��ʽ�ֱ�Ϊ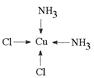 ��
��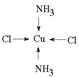 ��
��
�����Ѷȣ�һ��
3��ѡ���� ���в����ھ�����ص����
[? ]
A��һ���й���ļ�������
B��һ���и�������
C��һ���й̶����۵�
D��һ������ɫ���Ĺ���
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� ����˵����ȷ����:?��?��
A�������ᷴӦ�������һ���Ǽ���������
B��SiO2�����У�1��Siԭ����2��Oԭ���γ��������ۼ�
C�����Ӿ����з��Ӽ�������Խ�������Խ�ȶ�
D�����Ӿ�������ˮʱ�������еĻ�ѧ�����ܱ��ƻ�
�ο��𰸣�D
���������A��������������������ᣬ����Ϊ����������
B��SiO2�����У�1��Siԭ����4��Oԭ���γ��ĸ����ۼ�
C�����Ӽ�������һ��Ӱ����Ǿ�����ܷе㣬������ȶ���û��ֱ�ӹ�ϵ
D. ���Ӿ�������ˮʱ��ֻ���ƻ��ķ��Ӽ������������еĻ�ѧ�������ܱ��ƻ�
��ΪD
�����Ѷȣ�һ��
5��ѡ���� �������һ����ԭ�Ӻ�̼ԭ�ӹ��ɵ���̬�Ŵط��ӣ���ͼ��ʾ�����Ǻ����ĵ�ԭ������ԭ�ӣ�������ĺ����ĵ�ԭ����̼ԭ�ӣ����Ļ�ѧʽΪ 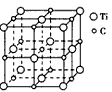
[? ]
A.Ti14C13
B.TiC
C.Ti4C4
D.Ti4C3
�ο��𰸣�A
���������
�����Ѷȣ�һ��