时间:2017-07-31 23:38:11
1、选择题 下列关于电解质溶液的叙述正确的是(? )
A.常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO-)>c(Na+)
B.稀释醋酸溶液,溶液中所有离子的浓度均降低
C.在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-)
D.0.1 mol・L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S)
参考答案:C
本题解析:由CH2COONa和CH3COOH混合液中的电荷守恒可知c(CH3COO-)=c(Na+),A错误;稀释醋酸时,c(H+)减小,但c(OH-)增大,B错误;Na2S溶液中存在质子守恒:c(OH-)=c(H+)+c(HS-)+2c(H2S),D错误;NaCl溶液中c(Na+)和c(Cl-)一定相等。
本题难度:一般
2、选择题 下列事实一定能说明HF是弱酸的是
[? ]
参考答案:D
本题解析:
本题难度:一般
3、填空题 请按要求完成下列各项填空:
(1)①pH=a的CH3COOH溶液稀释100倍后,所得溶液pH______a+2(填“>”或“<”).
②0.01mol/LCH3COOH溶液的pH______2(填“>”或“<”).
③0.1mol/LCH3COONa溶液的pH______7(填“>”或“<”).
(2)观察比较以上三个小题,试提出证明某酸(HA)是弱电解质的两种较稳妥的实验方法:
一是:______;
二是:______.
参考答案:(1)①CH3COOH是弱酸,存在电离平衡,加水促进电离,所以CH3COOH溶液稀释100倍后,pH变化小于2个单位,即所得溶液pH<a+2,故答案为:<;
②CH3COOH是弱酸,在水溶液中部分电离,所以溶液中氢离子浓度小于酸的浓度,所以0.01mol/L CH3COOH溶液的pH>2,故答案为:>;
③CH3COONa属于强碱弱酸盐,醋酸根离子在水溶液中水解显碱性,所以溶液的pH>7,故答案为:>;
(2)证明某酸(HA)是弱电解质的两种较稳妥是测定酸的PH或其盐溶液的pH,因为pH容易测定,
故答案为:测量0.01mol/LHA溶液的pH,若大于2则为弱电解质;测量0.1mol/L CH3COONa溶液的pH,若大于7则为弱电解质.
本题解析:
本题难度:一般
4、选择题 下列对各个图象的描述正确的是 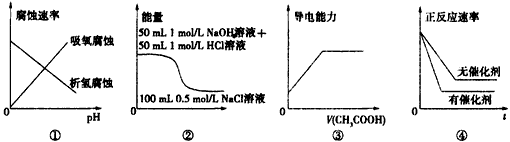
[? ]
A.图①表示析氢腐蚀、吸氧腐蚀速率与金属周围溶液pH的关系
B.图②表示物质能量的大小关系
C.图③表示在氨水中加入同浓度的醋酸溶液时导电能力变化情况
D.图④表示有无催化剂情况下正反应速率随时间变化的情况
参考答案:B
本题解析:
本题难度:一般
5、选择题 某氨水中c( )=0.5 mol / L时达到电离平衡,若向其中加入c(
)=0.5 mol / L时达到电离平衡,若向其中加入c( )=0.5 mol / L的NH4Cl溶液后,NH3・H2O的电离程度将?(?)
)=0.5 mol / L的NH4Cl溶液后,NH3・H2O的电离程度将?(?)
A.减少
B.不变
C.增大
D.无法判断
参考答案:C
本题解析:
正确答案:C
加入c( )=0.5 mol / L的NH4Cl溶液后,NH3・H2O的体积扩大一倍,NH3・H2O的平衡向电离方向移动,NH3・H2O的电离程度将境大。
)=0.5 mol / L的NH4Cl溶液后,NH3・H2O的体积扩大一倍,NH3・H2O的平衡向电离方向移动,NH3・H2O的电离程度将境大。
本题难度:简单