时间:2017-07-27 11:05:28
1、选择题 在常温下发生下列反应:
(1)16H++10Z-+2XO4-=2X2++5Z2+8H2O
(2)2A2++B2=2A3++2B-
(3)2B-+Z2=B2+2Z-
根据上述反应,判断下列结论中错误的是
[? ]
参考答案:B
本题解析:
本题难度:简单
2、选择题 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示。下列说法中不正确的是( )。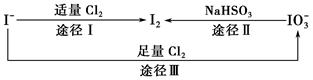
A.用淀粉—KI试纸和食醋检验加碘盐时淀粉—KI试纸会变蓝
B.足量Cl2能使湿润的、已变蓝的淀粉—KI试纸退色的原因可能是5Cl2+I2+6H2O=2HIO3+10HCl
C.由图可知氧化性的强弱顺序为Cl2>I2>IO3-
D.途径Ⅱ中若生成1 mol I2,则反应中转移的电子数为10NA
参考答案:C
本题解析:加碘盐中含有IO3-,在酸性条件下可被I-还原生成I2,A选项正确;根据图示转化关系可知B选项正确;根据途径I可知氧化性Cl2>I2,根据途径Ⅱ可知氧化性IO3->I2,根据途径Ⅲ可知氧化性Cl2>IO3-,C选项错误;根据关系式2IO3-~I2~10e-可知D选项正确。
本题难度:一般
3、选择题 有下列氧化还原反应:①Fe+CuSO4==Cu+FeSO4
②Cu+2FeCl3==CuCl2+2FeCl2 ③2FeCl2+Cl2==2FeCl3
根据上述反应可判断各粒子氧化性由强到弱的顺序正确的是
A.Cl2>Fe3+>Cu2+>Fe2+
B.Cl2>Cu2+>Fe2+>Fe3+
C.Fe3+>Cu2+>Cl2>Fe2+
D.Fe3+>Cl2>Cu2+>Fe2+
参考答案:A
本题解析:略
本题难度:一般
4、选择题 已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<
I-<SO2,则下列反应中不能发生的是
[? ]
A.H2O2 + H2SO4 ══ SO2 ↑ + O2 ↑ + 2H2O
B.I2 + SO2 + 2H2O ══ H2SO4 + 2HI
C.2Fe2+ + Cl2 ══ 2Fe3+ + 2Cl-
D.2Fe3+ + SO2 + 2H2O ══ 2Fe2+ + SO42-+ 4H+
参考答案:A
本题解析:
本题难度:一般
5、选择题 O3具有强氧化性,将O3通入KI溶液中发生反应:O3+I-+H+―→I2+O2+H2O(未配平),下列说法正确的是? ( )。
A.配平后的离子方程式为2O3+2I-+4H+=I2+2O2+2H2O
B.每生成1 mol I2转移电子2 mol
C.O2是还原产物之一
D.该反应能说明O2的氧化性大于I2的
参考答案:B
本题解析:A项中方程式虽然满足原子守恒,但不满足电子守恒和电荷守恒,配平后正确的离子方程式为O3+2I-+2H+=I2+O2+H2O,故每生成1 mol I2转移电子2 mol,A项错误, B项正确;O3和O2中O的化合价均为0,故O2既不是氧化产物,也不是还原产物,C项错误;该反应能说明O3的氧化性大于I2的,而不能说明O2的氧化性大于I2的,D项错误。
本题难度:一般