ʱ��:2017-07-27 10:26:19
1��ѡ���� ��ϸ�մ����ִ��Ƽ����й㷺��Ӧ�ã���SnO2������PbCl2��ĥ�ɼ�ϸ�Ŀ������������ս�ɶ���壬���а뵼������ʲ����нϴ�ı�����������͵���Ԫ�����DZ���ɵĵ��ӱDZ���Ϊ���˹���ǡ������������в���ȷ��Ϊ��?��
A�����˹���ǡ����ͻ�����˵����
B�����˹���ǡ����������������ǿ
C�����˹���ǡ��㷺������ȼ���ױ����ж�������Զ����ͱ���
D�����˹���ǡ�������ˮ
�ο��𰸣�D
������������˹���ǡ���ף��нϴ���������������壻���а뵼�����ʣ����ܼ���˵�����о��������ж����岢������
�����Ѷȣ���
2��ѡ���� �豻��Ϊ���ǽ������ϵ����ǡ�������Ʒ�õ��赥�ʵ���
A���մɲ;�
B��ʯӢ�ӱ�
C�������оƬ
D�����ά
�ο��𰸣�C
���������A���մɲ;��ǹ����β�Ʒ������B��ʯӢ�ӱ��Ƕ��������Ʒ������C�������оƬ�Ǹߴ��ȵĹ��Ʒ����ȷ��D�����ά���Ƕ��������Ʒ������
�����Ѷȣ���
3������� A��B��C��D�ǰ�ԭ��������С�������еĵ�2��3���ڵ�Ԫ�صĵ��ʡ�B��E��Ϊ��ɿ����ijɷ֡�F����ɫ��Ӧ�ʻ�ɫ����G�У��ǽ���Ԫ�������Ԫ�ص�ԭ�Ӹ�����Ϊ1��2����һ�������£�������֮����ת����ϵ���£�ͼ�в��ֲ���δ�г�����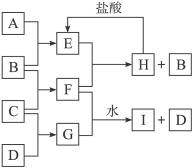
����д���пհף�
��1��A��______________________��C��______________________��
��2��H�����ᷴӦ����E�Ļ�ѧ����ʽ��______________________________________��
��3��E��F��Ӧ�Ļ�ѧ����ʽ��______________________________________________��
��4��F��G��ˮ��Һ��Ӧ����I��D�����ӷ���ʽ��____________________________��
�ο��𰸣�(1)̼����C��?�ƣ���Na��
(2)Na2CO3+2HCl====2NaCl+H2O+CO2��
(3)2CO2+2Na2O2====2Na2CO3+O2
(4)Na2O2+S2-+2H2O====4OH-+S+2Na+
��������������е���Ҫ�ɷ���N2��O2��CO2��F����ɫ��Ӧ�ʻ�ɫ��˵��������Ԫ�ء�H�������ᷴӦ����E����֪EΪCO2��BΪO2��FΪNa2O2��HΪNa2CO3��CΪNa��AΪC������Na��D��Ӧ����Na2D����D���ڵ�2��3����Ԫ�صĵ��ʣ���G����Na2O2��Ӧ��Na2D��������Na2O��ֻ������Na2S��Na2S�е�S2-���бȽ�ǿ�Ļ�ԭ�ԣ��ܱ�Na2O2������S��Na2O2+S2-+2H2O====4OH-+S+2Na+��
�����Ѷȣ���
4��ѡ���� ��ʯ��(crocidolite)������������֯ȷ�ϵ�һ���°����ʣ��ǡ�¹�ص���Լ���������Ƶ�46�ֻ�ѧƷ֮һ����ʯ�Ļ�ѧʽΪNa2Fe5Si8O22(OH)2����ʯ����ϡ���ᴦ��ʱ����ԭ����ֻ��NO������˵������ȷ����(����)��
A����ʯ����һ����ȼƷ����������ˮ
B����ʯ�Ļ�ѧ��������������ʽ�ɱ�ʾΪ��Na2O��3FeO��Fe2O3��8SiO2��H2O
C��1 mol Na2Fe5Si8O22(OH)2���������������ã�����������8.5 L 2 mol��L��1 HNO3��Һ
D��1 mol Na2Fe5Si8O22(OH)2��������������ã�����������7 L 2 mol��L��1 HF��Һ
�ο��𰸣�B
�����������ʯ�Ȳ���ȼ�գ�Ҳ������ˮ����Na2Fe5Si8O22(OH)2��д�����������ʽ����ΪNa2O��3FeO��Fe2O3��8SiO2��H2O�����е�Na2O��FeO��Fe2O3��SiO2����������ᷢ�����ֽⷴӦ����Na2O��Fe2O3�������ᷢ�����ֽⷴӦ��FeO�����ᷢ��������ԭ��Ӧ��3FeO��10HNO3=3Fe(NO3)3��NO����5H2O��SiO2�������Ӧ������1 mol��ʯ���и���������HF��NHO3��Ӧ���������Ӧʱ�����ʵ���֮�ȿ��ж�C��D����
�����Ѷȣ�һ��
5��ѡ���� ����һ�ִ�����Fe��Si�������ʡ�ȡ����������Ʒ���ֱ�Ͷ��������ϡ��������������У���ַ�Ӧ�ų�������������������е�����Ĺ�ϵ��
A�����ʵ���֮��Ϊ1��1
B�����ʵ���֮��Ϊ2��1
C������֮��Ϊ1��1
D������֮��Ϊ2��1
�ο��𰸣�B
�����������Ӧ2Al+6HCl�T2AlCl3+3H2����2Al+2NaOH+2H2O�T2NaAlO2+3H2����
�����������Ʒ�ֱ�Ͷ��������ϡ���������������Һ�У���ַ�Ӧ�ų�������������
��ӦFe+2HCl�TFeCl2+H2����Si+2NaOH+H2O�TNa2SiO3+2H2�������ɵ�������ͬ��
��������2molH2��n��Fe��=2mol��n��Si��=1mol��
���������������ʵ�����Ϊ2mol��1mol=2��1������֮��Ϊ4��1��
��ѡB��
���������⿼��Al��Fe��Si�Ļ�ѧ���ʣ���ȷ�����Ļ�ѧ��Ӧ����Ϣ����������������ͬ�ǽ����Ĺؼ����ѶȲ���
�����Ѷȣ���