ʱ��:2017-07-27 09:59:56
1������� ������Դ����Ľ�һ��ͻ���������Ȼ�ѧѭ��������о��ܵ��������ҵ�������������о����֣��������������̣�MnFe2O4��Ҳ�������Ȼ�ѧѭ���ֽ�ˮ���⣬MnFe2O4���Ʊ��������£�
��1��ԭ��Fe��NO3��n��n=______��Ͷ��ԭ��Fe��NO3��n��Mn��NO3��2�����ʵ���֮��ӦΪ______��
��2��������С��������衱��Ŀ����______����������ϴ�Ӹɾ��ı���______��
��3������MnFe2O4�Ȼ�ѧѭ������ķ�Ӧ�ɱ�ʾΪ��MnFe2O4
| x 2 |
�ο��𰸣���1��MnΪ+2�ۣ���MnFe2O4��Fe�Ļ��ϼ�Ϊa�ۣ����ݻ��ϼ۴�����Ϊ0����2+2a+4����-2��=0�����a=+3����Fe��NO3��n��n=3��
��MnFe2O4��ɿ�֪��Fe��Mn�ĸ���֮��Ϊ1��2�����������غ��֪��Fe��NO3��n��Mn��NO3��2 ����֮�� 2��1��
�ʴ�Ϊ��3��2��1��?
��2������������Ϊ���ö��߳�ַ�Ӧ���������ܸ���KOH�ȣ�ϴ�������ԣ�˵��ϴ�Ӹɾ�����֤���﴿����
�ʴ�Ϊ����ַ�Ӧ�������ȫ��ϴ��������Һ�����ԣ�
��3����x=0.8ʱ�������ܼ�̬Ϊ��4-0.8����2-2=4.4����1mol MnFe2O4-0.8�к�Fe2+��Fe3+���ʵ����ֱ�Ϊxmol��ymol������x+y=2��2x+3y=4.4��������ã�x=1.6��y=0.4��
��1mol MnFe2O4-0.8�к�Fe2+�����ʵ���Ϊ1.6mol����Fe2+ռ�İٷ���Ϊ1.6mol2mol��100%=80%��
�ʴ�Ϊ��80%��
��������ͼ���Կ������̼���Լ����������Ⱦ���������۲���ѭ��ʹ�ü������������ڲ�ͬ�������ɣ������ڸ���������������ȣ�
�ʴ�Ϊ�����̼���Լ����������Ⱦ���������۲���ѭ��ʹ�ü������������ڲ�ͬ�������ɣ������ڸ���������������ȣ�
���������
�����Ѷȣ�һ��
2��ѡ���� ���з��뷽������ȷ���ǣ�������
A���ù��˵ķ�����ȥʳ��ˮ�е���ɳ
B��������ķ���������ˮ�Ƴ�����ˮ
C�������Ȼ�̼��ȡ��ˮ�еĵ�
D���÷�Һ©���������ͺ�ֲ����
�ο��𰸣�A��ʳ��ˮ�е���ɳ���������ʣ����벻�������Һ���ù��˵ķ�������A��ȷ��
B������ˮ�к����ѻӷ������ʣ���ͨ���������룬��B��ȷ��
C���ⵥ���������л��ܼ����Ȼ�̼����ͨ����ȡ�������룬��C��ȷ��
D�����ͺ�ֲ�����ǻ��ܵ��������ʣ�������ķ��벻�ܲ��÷�Һ������D����
��ѡD��
���������
�����Ѷȣ�һ��
3������� ����ȥ�±��и���ĩ״������е����ʣ�������Ϊ���ʣ�������д���õ��Լ����������Ƽ���ѧ����ʽ�� 
�ο��𰸣�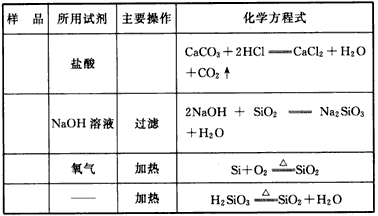
���������
�����Ѷȣ�һ��
4��ѡ���� ij������FeCl3��Һ��ʴ����ͭ�ľ�Ե������ӡˢ��·����֪�����ķ�ӦΪ 2FeCl3 + Cu =2FeCl2 + CuCl2��������С��Ϊȷ��������ķ�Һ����ɣ���������ʵ�飺
��1��ȡ100 mL��Һ����������AgNO3��Һ�����ɳ��� 86.1g��
��2����ȡ100 mL��Һ����ͭƬ��ַ�Ӧ��ͭƬ����������2.56 g��
���й���ԭ��Һ��ɵ��жϴ������
A.c(Fe2+)�Uc(Fe3+)�Uc(Cu2+) = 2�U1 �U1
B.c(Fe2+)�Uc(Cu2+) = 2�U1
C.һ������Fe 2+��Fe 3+��Cu2+��Cl��
D.c(Cl��) =6mol / L��c(Fe 2+) = 1.2mol / L
�ο��𰸣�A
��������������������1��������AgClΪ86.1g����0.6mol��n(Cl��)=0.6mol��c(Cl��)= 6mol/L�� n(Fe3+)=0.2mol����c(Fe3+)=2 mol/L��
��2��ͭƬ����������2.56 g�����μӷ�Ӧ��ͭ�����ʵ���Ϊ0.04mol�����ݻ�ѧ����ʽ���㣬100 mL��Һ�л���FeCl3�����ʵ���Ϊ0.08mol��
�ۺ����Ϸ�����100 mL��Һ��n(Fe3+)=0.2mol����Ӧ��n(Fe3+)=0.12mol�����ݻ�ѧ����ʽ���㣬��Һ�е����ʵ���Ϊ��n(Fe2+)=0.12mol��n(Cu2+)=0.6mol��Ũ�ȷֱ�Ϊ��c(Fe2+)=1.2 mol / L��c(Fe3+)="0.8" mol / L��c(Cu2+)="0.6" mol / L��
A��c(Fe2+)�Uc(Fe3+)�Uc(Cu2+)? = 1.2�U0.8�U0.6=6��4��3���ʴ���
��ѡA��
���㣺���κ������ε��ת�� ��ѧ����
���������⿼���˽������˳���Ӧ�ã���ɴ��⣬�������ݽ������˳����������У�Ҫע���������ͭ�Ļ��ǿ��ȷ����Ӧ���Ⱥ�˳��
�����Ѷȣ���
5��ѡ���� ����������Һ�����Ȼ��ƺ͵������ˮ��Һ?�����ͺ��Ȼ�����Һ
��19%���Ҵ���Һ���������ϸ����Һ����ȷ����һ���ǣ�?��
A����ȡ����Һ������
B����Һ����ȡ������
C����ȡ������Һ
D������Һ����ȡ
�ο��𰸣�A
�����������ȡ�ʺ��������ڲ�ͬ�ܼ��е��ܽ��Բ�ͬ�������һ�ַ�������Һ�����ڻ������ܵ�Һ��֮���һ�ַ��뷽�������������ݻ�����и���ַе㲻ͬ�������һ�ַ��������ڳ�ȥ�ӷ����ѻӷ��ӷ����ʡ��������������л��ܼ��У���ȡ���ɣ����Ͳ�����ˮ����Һ���ɣ��Ҵ���ˮ���ܣ����ɣ����Դ�ѡA��
�����Ѷȣ���