时间:2017-07-27 09:38:21
1、选择题 下列叙述正确的是
[? ]
参考答案:B
本题解析:
本题难度:简单
2、选择题 将一定量的MgCl2溶于90g水中,使每100个水分子中有一个Cl-,这一定量MgCl2的物质的量为( )
A.0.09mol
B.0.025mol
C.0.05mol
D.0.1mol
参考答案:B
本题解析:
本题难度:简单
3、简答题 [选做题](1)人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程.目前中学课本中的酸碱理论是1889年阿仑尼乌斯(Arrhenius)提出的电离理论.
①1905年富兰克林(FranKlin)深入研究了水和液氨的相似性,把阿仑尼乌斯以水为溶剂的个别现象,推广到任何溶剂,提出了酸碱溶剂理论.溶剂理论认为:凡能电离而产生溶剂正离子的物质为酸,凡能电离而产生溶剂负离子的物质为碱.试写出液氨自身电离的方程式:______.
②1923年丹麦化学家布朗斯特(Bronsted)和英国化学家劳莱(Lowey)提出质子理论.凡是能够释放质子(氢离子)任何含氢原子的分子或离子都是酸;凡是能够与质子(氢离子)结合的分子或离子都是碱.
按质子理论:下列粒子在水溶液既可以看作酸又可看碱的是______.
A、H2O?B、NH4+?C、OH-?D、HCO3-?E、CH3COO-?F、Cl-
③1923年路易斯(Lewis)提出广义的酸碱概念.凡是能给出电子对而形成化学键的物质都是碱;凡是能够和电子对结合的物质都是酸.
酸(电子对接受体)+碱(电子对给予体)→反应产物,如:H++OH-→H2O.
试指出下列两个反应中的酸或碱:
(Ⅰ)H3BO3+H2O?
H++B(OH)4-,该反应中的碱是______(填H3BO3或H2O);
(Ⅱ)NaH+H2O═NaOH+H2↑,该反应中的酸是______(填NaH?或H2O).
(2)已知A元素原子的K、L层电子数之和比M、L层电子数之和多一个电子;B元素原子核外电子占有9个轨道,且有1个未成对电子;C元素原子核外3p亚层中3个轨道还需5个电子才能达到全充满.D元素只有两个电子层,且最高化合价与最低化合价的代数和为零;E原子半径最小;F元素最外层电子排布为nSnnPn+1.按要求填写
①B的电子排布式是:______,A、B两元素形成的化合物的晶体类型是______.
②D元素单质的晶体类型是______,C单质的制备方法是:______.
③E和F形成的化合物空间构型为______,该物质比D与E形成的化合物更容易液化的原因是______.
参考答案:(1)①水分子电离出水合氢离子和氢氧根离子,利用类比法,液氨自身电离的方程式2NH3=NH4++NH2-.
故答案为:2NH3=NH4++NH2-.
?②根据质子理论分析,电离出氢离子的是酸,结合氢离子的是碱;
A、H2O?D、HCO3-?既能电离出氢离子,又能结合氢离子,所以既可以看作酸又可看作碱;
B、NH4+? 能电离出氢离子,所以是酸;
C、OH-、E、CH3COO-、F、Cl- 能结合氢离子,所以是碱.
故答案为:A?D.
③根据广义酸碱概念分析,凡是能给出电子对而形成化学键的物质都是碱;凡是能够和电子对结合的物质都是酸;
(Ⅰ)H3BO3+H2O?
H++B(OH)4-,该反应中给出电子对而形成化学键的物质H2O,所以该反应中的碱是H2O.
故答案为:H2O.
(Ⅱ)NaH+H2O═NaOH+H2↑,该反应中和电子对结合的物质H2O,所以水是酸.
故答案为:H2O.
(2)根据题意知,A元素有3个电子层,最外层有7个电子,所以A是Na;B元素原子核外电子占有9个轨道,且有1个未成对电子,由此判断B是Cl;C元素原子核外3p亚层中3个轨道还需5个电子才能达到全充满,所以C元素的3P亚层有1个电子,所以C是Al;D元素只有两个电子层,且最高化合价与最低化合价的代数和为零,主族元素的族序数=其最外层电子数,最高正化合价+最低负化合价的绝对值=8,所以D是C;E原子半径最小,所以E是H;F元素最外层电子排布为nSnnPn+1,S能级最多排2个电子,故n是2,所以F元素最外层电子排布为2S22P3,所以是N.
①通过以上分析知,B是Cl,所以其核外电子排布式为1s22s22p63s23p5;A是Na,B是Cl,活泼金属和活泼非金属元素之间形成离子键,所以是离子晶体;
故答案为:1s22s22p63s23p5;?离子晶体.
?②D是C元素,碳单质的晶体类型是原子晶体;C单质是Al,活泼金属采用电解法冶炼.
故答案为:原子晶体;?电解法.
③E是H元素,F是N元素,所以形成的化合物是NH3,NH3的空间构型为三角锥型;NH3分子间能形成氢键,所以容易液化.
故答案为:三角锥型;?E和F形成的化合物分子间能形成氢键.
本题解析:
本题难度:一般
4、实验题 已知Ca(OH)2、CaCO3和Ca(HCO3)2都是电解质,进行如图所示的实验,请将实验现象填入下表中的空格处。 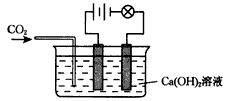
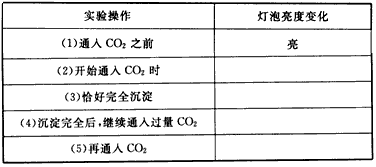
参考答案:(2)变暗;(3)熄灭;(4)又变亮;(5)明亮程度几乎不变
本题解析:
本题难度:一般
5、选择题 有①Na2CO3溶液;②CH3C00Na溶液;③NaOH溶液各25mL,物质的量浓度均为0.1 mol/L,
下列说法正确的是
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25mL 0.1 mol/L盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
参考答案:C
本题解析:试题分析:A错误,③最大,因为氢氧化钠是强碱,完全电离。前两者都是弱电解质,酸根离子对应的酸的酸性越弱,相应的该酸根离子水解程度越大,所以相同浓度的碳酸钠水解程度比醋酸钠大,即pH①>②。顺序应该是③>①>②。B错误,变化最大的应该是氢氧化钠,因为加水稀释会促进水解,则弱盐溶液的pH变化就小。C正确,加入25mL 0.1 mol/L盐酸后,氢氧化钠溶液最终变为氯化钠溶液,室温时pH是7。醋酸钠溶液最终变为醋酸与氯化钠的混合溶液,室温时pH小于7.碳酸钠溶液最终变为碳酸氢钠溶液,室温时pH大于7。综上,pH最大的是①。D错误,pH相同的情况下,浓度的大小应该是A中顺序的倒序,即②<①<③。
考点:盐水解的影响因素
本题难度:简单