时间:2017-07-27 09:17:29
1、填空题 有一包白色固体,可能含有NaCl、Na2SO4、CaCl2、CuSO4、Na2CO3 和CaCO3 ,将固体放入水中,经搅拌后为无色溶液,在溶液里加入BaCl2 溶液,产生白色沉淀,再加入盐酸,沉淀全部消失并有气体放出,由此推断:
(1)原固体肯定有______________。
(2)原固体肯定不存在?。
(3)__________不能确定存在与否,要确定其存在,应进行的实验是_?__。
参考答案:(1)Na2CO3?(2)Na2SO4? CaSO4? CuSO4? CaCO3? (3)NaCl;
取少许固体溶于水,然后加入过量硝酸,再加入硝酸银溶液,若有白色固体生成则原固体中含有氯化钠
本题解析:略
本题难度:一般
2、选择题 元素周期表中部分短周期元素的位置如图所示,其中A元素最外层电子数是其电子层数的2倍.下列有关A、B、C、D、E五种元素的叙述不正确的是( )
A.A与B形成的阴离子可能有AB32-、A2B42-
B.E的氢化物的沸点比C的氢化物的沸点高
C.A在过量的B2中燃烧的主要产物为AB2
D.A与E形成的化合物是非极性分子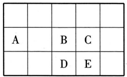
参考答案:A元素最外层电子数是其电子层数的2倍,则A元素原子有2个电子层,最外层电子数为4,故A为碳元素,由A、B、C、D、E五种元素在短周期中的相对位置可知,B为氧元素,C为氟元素,D为硫元素,E为氯元素,
A、A为碳元素,B为氧元素,碳元素与氧元素可以形成碳酸根离子(CO32-)、草酸根离子C2O42-,故A正确;
B、氟化氢分子中存在氢键,氢键比分子间作用力强,氟化氢的沸点高于氯化氢,故B错误;
C、碳在足量的氧气中燃烧生成二氧化碳,故C正确;
D.A与E形成的化合物是四氯化碳,为正四面体结构,是对称结构,正电荷重心与负电荷重心重合,为非极性分子,故D正确;
故选B.
本题解析:
本题难度:简单
3、选择题 门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第4周期的三种元素留下了空位,并对它们的 一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是
[? ]
A.X单质不易与水反应
B.XO2可被碳或氢气还原为X
C.XCl4的沸点比SiCl4的高
D.XH4的稳定性比SiH4的高
参考答案:D
本题解析:
本题难度:简单
4、选择题 X、Y、Z、W有如下图所示的转化关系,则X、Y可能是(?)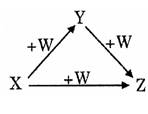
①C、CO?②AlCl3、Al(OH)3
③Fe、FeCl3?④Na2CO3、NaHCO3
A. 只有①②? B. 只有③④
C. 只有①②④? D. ①②③④
参考答案:C
本题解析:略
本题难度:一般
5、填空题 元素的分区和族
(1)s 区: ,最后的电子填在_______上,包括_________,属于活泼金属,为碱金属和碱土金属;
,最后的电子填在_______上,包括_________,属于活泼金属,为碱金属和碱土金属;
(2)p区: ;最后的电子填在_______上,包括_______族元素,为非金属和少数金属;
;最后的电子填在_______上,包括_______族元素,为非金属和少数金属;
(3)d区: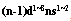 ,最后的电子填在_______上,包括_______族元素,为过渡金属;
,最后的电子填在_______上,包括_______族元素,为过渡金属;
(4)ds区: ?, (n-1)d全充满, 最后的电子填在_______上,包括_______,过渡金属(d和ds区金属合起来,为过渡金属);
?, (n-1)d全充满, 最后的电子填在_______上,包括_______,过渡金属(d和ds区金属合起来,为过渡金属);
(5)f区: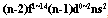 ,包括_______元素,称为内过渡元素或内过渡系。
,包括_______元素,称为内过渡元素或内过渡系。
参考答案:(1)ns;IA和IIA族元素
(2)np;IIIA-VIIA族、零族元素
(3)(n-1)d;第IIIB族到VIII族元素
(4)ns;IB族和IIB族元素
(5)镧系和锕系元素
本题解析:
本题难度:一般