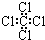时间:2017-07-27 09:08:36
1、填空题 (8分)下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种气体,C的相对分子质量为78。请回答相关问题: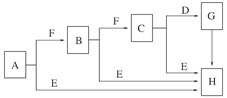
(1)下列对C的结构、性质推断不正确的是( )
A.久置于空气中会变成白色
B.具有强氧化性
C.晶体中存在离子键与非极性键
D.是一种碱性氧化物
(2)A的原子结构示意图为________,H的电子式为________,E的结构式为________。
(3)C和E反应生成H的离子方程式为________,反应中氧化剂与还原剂的物质的量之比为________。
2、选择题 下面的叙述正确的是?
[? ]
A.两种非金属元素原子之间形成的化学键不一定都是极性键
B.共价化合物中可能含有离子键
C.只要是离子化合物其熔点就比共价化合物的熔点高
D.将某种化合物溶于水,若能导电说明这种化合物是离子化合物
3、填空题 前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。回答下列问题: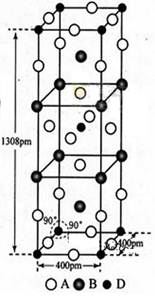
(1)D2+的价层电子排布图为_______。
(2)四种元素中第一电离最小的是________,电负性最大的是________。(填元素符号)
(3)A、B和D三种元素责成的一个化合物的晶胞如图所示。
①该化合物的化学式为_________;D的配位数为_______;
②列式计算该晶体的密度_______g・cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_____;该化合物中存在一个复杂离子,该离子的化学式为_______,配位体是____。
4、填空题 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是________(用对应的元素符号表示);D原子的基态电子排布式为____________________________________________________。
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取________杂化;BC的空间构型为________(用文字描述)。
(3)1 mol AB-中含有的π键个数为________。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比是________。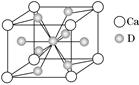
(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=________(填数值);氢在合金中的密度为________。
5、选择题&nbs来源:91考试网 91exam.orgp; 下列化学用语正确的是( ? )
A.聚丙烯的结构简式为: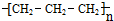
B.乙烯的结构简式:CH2CH2
C.CH4分子的比例模型:
D.四氯化碳分子的电子式为: