时间:2017-07-27 08:54:47
1、选择题 下列溶液中各微粒的浓度关系一定正确的是( ? )
A.碳酸溶液中,H2CO3第一级电离出H+的是第二级电离出H+的2倍
B.在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.25℃时,pH=10的CH3COONa溶液与pH=l0的氨水中,由水电离出的c(OH-)之比为1:1
D.物质的量浓度相同的4种溶液①CH3COONa②NaNO3③Na2CO3④NaOH,pH的大小顺序是④>③>①>②
参考答案:D
本题解析:
本题难度:简单
2、选择题 关于小苏打水溶液的表述正确的是( )
A.HCO3-的电离程度大于HCO3-的水解程度
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
D.存在的电离有:NaHCO3═Na++HCO3-,HCO3-?H++CO32-,H2O?H++OH-,HCO3-+H2O?H2CO3+OH-
参考答案:A、碳酸氢根离子电离显酸性,碳酸氢钠溶液呈碱性,说明碳酸氢根离子水解程度大于电离程度,故A错误;
B、溶液中存在物料守恒,由碳元素守恒可知c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故B正确;
C、溶液中存在电荷守恒,由阴阳离子电荷守恒可知c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故C错误;
D、存在的电离有:NaHCO3═Na++HCO3-,HCO3-?H++CO32-,H2O?H++OH-,反应HCO3-+H2O?H2CO3+OH-是盐类水解反应,不是电离方程式,故D错误;
故选B.
本题解析:
本题难度:简单
3、选择题 常温下,用0.100?0?mol/L?NaOH溶液滴定20.00?mL?0.100?0?mol/L?CH3COOH溶液所得滴定曲线如图所示.下列说法正确的是? 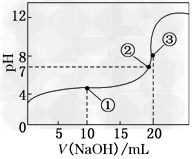
[? ]
A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
参考答案:D
本题解析:
本题难度:一般
4、选择题 在蒸发皿中加热蒸干下列物质的溶液并灼烧,可得原有物质的固体是( ? )
A.氯化铝
B.碳酸氢镁
C.硫酸亚铁
D.碳酸钠
参考答案:D
本题解析:
本题难度:简单
5、填空题 (1)0.020mol/L的HCN(aq)与0.020mol/L NaCN(aq)等体积混合,已知该混合溶液中c[Na+]>
c[CN-],用“>、<、=”符号填空
①溶液中c[OH-]__________c[H+] ②c[HCN]_________c[CN-]
(2)向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再生成二氧化碳气体为止,则在此过程中,溶液的碳酸氢根离子浓度变化趋势可能是:(A) 逐渐减小; (B) 逐渐增大; (C) 先逐渐增大,而后减小;(D) 先逐渐减小,而后增大。你的选择是__________
(3)pH值相同的 ①HCl(aq)、 ②H2SO4(aq)、 ③CH3COOH(aq)各100 mL
①三种溶液中物质的量浓度最大的是__________(化学式)。
②分别用0.1 mol/L的NaOH(aq)中和,其中消耗NaOH(aq)最多的是(化学式)__________。
③分别投入足量大小相同的锌粒,反应开始时,反应速率__________。
A、HCl最快 B、H2SO4最快 C、CH3COOH最快 D、一样快
(4)某温度下,纯水中的c[H+] = 2.0×10-7mol/L,则此时c(OH-)=__________mol/L。相同条件下,测得
① NaHCO3(aq)② CH3COONa(aq)③ NaClO(aq)三种稀溶液的pH值相同。那么,它们的物质的量浓度由大到小的顺序是_________________。
(5)25℃时, 0.05mol/LH2SO4溶液的PH=_________;0.05mol/LBa(OH)2溶液C(H+)=_______ mol/L
参考答案:(1)① >;② >
(2)C
(3)①CH3COOH(aq);② CH3COOH(aq);③ D
(4)2.0×10-7mol/L;②①③
(5)1;1×10-13
本题解析:
本题难度:一般