时间:2017-07-27 08:42:52
1、选择题 煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s) + CO(g) CaO(s) + SO2(g) + CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaO(s) + SO2(g) + CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaSO4(s) + 4CO(g) CaS(s) + 4CO2(g) ΔH2=-175.6kJ·mol-1(反应Ⅱ)
CaS(s) + 4CO2(g) ΔH2=-175.6kJ·mol-1(反应Ⅱ)
假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是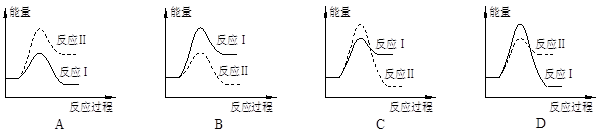
参考答案:C
本题解析:反应Ⅰ为吸热反应,反应Ⅱ为放热反应,则A、D错误;反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则反应Ⅱ的活化能较大,则B错误、C正确,故答案为:C。
考点:本题考查化学反应与能量转化、反应速率。
本题难度:一般
2、选择题 已知如下两个热化学反应方程式:
下列说法错误的是
A.反应①、②都属于加成反应
B.1,3—环己二烯比苯稳定
C.反应①、②的热效应说明苯环中含有的并不是碳碳双键
D.反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同
参考答案:B
本题解析:A、根据反应前后有机物结构变化可知,反应均是加成反应,A正确;B、反应①是吸热反应,这说明苯的能量一定低于1,3—环己二烯的能量,能量越低越无色,所以稳定性强的是苯,B错误;C、苯与氢气加成生成1,3—环己二烯是吸热反应,而1,3—环己二烯与氢气加成生成环己烷是放热反应,这说明苯环中含有的并不是碳碳双键,C正确;D、苯使溴水褪色发生的是萃取,属于物理变化,1,3—环己二烯含有碳碳双键与溴水发生加成反应而褪色,D正确,答案选B。
考点:考查有机物结构与性质以及反应热应用等
本题难度:一般
3、填空题 随着环保意识的增强,清洁能源越来越受人们关注。
(1)甲烷是一种洁净能源,已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802.3 kJ/mol
H2O(l)=H2O(g) △H=+44 kJ/mol
则4.8 g甲烷气体燃烧生成液态水放出的热量为_________________
(2)利用甲烷与水反应制备氢气,因原料价廉产氢率高,具有实用推广价值,已知该反应为:
CH4(g) +H2O(g)=CO(g) +3H2(g) △H=+206.1 kJ/mol
①若800℃时,反应的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=3.0 mol/L;c(H2O)=8.5 mol/L;c(CO)=2.0 mol/L;c(H2) =2.0 mol/L,则此时正逆反应速率的关系是___(填序号)。
A.v正>v逆 B.v正<v逆 C.v正=v逆 D.无法判断?
②若将温度降至600℃,此时平衡常数为K2,则K1 ___K2(填“>”、“<”或“=”)。?
(3)利用MnFe2O4作催化剂,通过两步反应可将水分解制得H2,第一步反应为:
MnFe2O4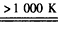 MnFe2O4-x+x/2_______
MnFe2O4-x+x/2_______
则框内物质为:_____________,第二步反应方程式为:________________________
参考答案:(1)267.1kJ(或267. 09kJ)
(2)①A;②>
(3)O2;MnFe2O4-x+xH2O=MnFe2O4+xH2↑
本题解析:
本题难度:一般
4、选择题 下列离子反应方程式正确的是
A.小苏打溶液中加入过量石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
B.氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+
C.氯化亚铁溶中通入氯气:Fe2++Cl2=Fe3++2Cl-
D.苛性钾溶液中加入稀醋酸:H++OH-=H2O
参考答案:B
本题解析:分析:A.小苏打溶液中加入过量石灰水,由于Ca2+过量,则溶液中不存在CO32-;
B.NH3?H2O为弱碱,与氯化铝反应只生成Al(OH)3;
C.电荷不守恒;
D.醋酸为弱电解质.
解答:A.小苏打溶液中加入过量石灰水,由于Ca2+过量,则溶液中不存在CO32-,反应的离子方程式为
HCO3-+Ca2++OH-=CaCO3↓+H2O,故A错误;
B.NH3?H2O为弱碱,与氯化铝反应只生成Al(OH)3,反应的离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B正确;
C.氯化亚铁溶中通入氯气反应的离子方程式应为2Fe2++Cl2=2Fe3++2Cl-,故C错误;
D.醋酸为弱电解质,应写成化学式,反应的离子方程式为OH-+CH3COOH=CH3COO-+H2O,故D错误.
故选B.
点评:本题考查离子方程式的书写,题目难度中等,本题注意A,为易错点,注意反应物的过量问题.
本题难度:一般
5、填空题 (6分)有下列七种物质:①Cl2?②Na2O2?③H2O2 ?④NH4Cl ?⑤CH4 ?⑥NaHSO4 ?⑦Ne?
回答下列问题
(1)不存在化学键的是_______________;(填序号)
(2)含有极性键和非极性键的是_______________;(填序号)
(3)NaHSO4固体溶于水,破坏了_____________键;其电离方程式为______________________
参考答案:(1)⑦(1分) (2)③(1分)(3) 离子键 极性共价键;? NaHSO4=Na++H++SO42-(每空2分)
本题解析:稀有气体⑦为单原子分子,不存在化学键;③H2O2中两个O原子间以非极性键结合,H和O之间靠极性键结合;NaHSO4固体溶于水,破坏的既有离子键又有极性共价键,电离方程式为NaHSO4=Na++H++SO42-。
本题难度:一般