时间:2017-07-27 08:37:48
1、选择题 下列有关0.1 mol・L-1 NaHCO3溶液中离子浓度的关系式,正确的是
[? ]
A.c(Na+) > c(HCO3-) > c(CO32-) > c(H+) > c(OH-)
B.c(Na+) > c(CO32-) > c(HCO3-) > c(OH-) > c(H+)
C.c(Na+)= c(HCO3-) + 2c(CO32-) + c(H2CO3)
D.c(Na+) + c(H+)?= c(HCO3-) + 2c(CO32-) + c(OH-)
2、填空题 (1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为______________(填序号)。
A.9 B.13 C.11~13之间 D.9~11之间
(2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)______________。
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH-)减小
(3)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①_________和__________两种粒子的物质的量之和等于0.1mol。
②_________和__________两种粒子的物质的量之和比OH-多0.05mol。
(4)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
① 若溶液中只溶解了一种溶质,该溶质的名称是____________,上述离子浓度大小顺序关系中正确的是
______________(选填序号) 。
② 若上述关系中C是正确的,则溶液中溶质的化学式是______________。
③ 若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)__________(填“>”、“<”、或“=”,下同) c(NH3・H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)
___________ c(Cl-)。
3、简答题 某温度下0.1mol/L?Na2CO3溶液中,[Na+]/[CO32-]=20/9>2,其原因是______,现向Na2CO3溶液中通入一定量的CO2后,[Na+]/[CO32-]=5/2>20/9,其原因是______,此时[HCO3-]=______.
4、选择题 下列说法正确的是
[? ]
A.?用甘氨酸(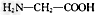 )和丙氨酸(
)和丙氨酸(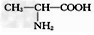 )缩合最多可形成4种二肽
)缩合最多可形成4种二肽
B.?0.1?mol/L?Na2S溶液中:c(OH-)=?c(H+)+?c(HS-)+?c(H2S)
C.?标准状况下,2.24L己烷含有分子的数目为0.1NA
D.?由离子方程式 +?XO3-?+?6H+?==?3X2?+?3H2O可判断X元素的最高化合价为+5价
+?XO3-?+?6H+?==?3X2?+?3H2O可判断X元素的最高化合价为+5价
5、填空题 现有浓度均为0.1?mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)______.
(2)④、⑤、⑦、⑧四种溶液中NH4+浓度由大到小的顺序是(填序号)______.
(3)将①和⑧等体积混合后,混合液中各离子浓度关系正确的是______.
A.c(H+)>c(SO42- )>c(NH4+)>c(OH-)
B.c(H+)=c(SO42- )=c(NH4 +)>c(OH-)
C.c(NH4+ )>c(H+)=c(SO42- )>c(OH-)
D.c(OH-)>c(H+)>c(NH4+)=c(SO42- )