时间:2017-07-27 08:11:43
1、选择题
A.A>B
B.A=10-4 B
C.B=10-4A
D.A=B
参考答案:B
本题解析:本题有两种解法。
方法1(常规解法):NaOH(aq)中:
c水(OH-)=c水(H+)=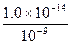 mol・L-1=1.0×10-5 mol・L-1
mol・L-1=1.0×10-5 mol・L-1
CH3COONa(aq)中:
c′水(OH-)=c′总(OH-)=10-9 mol・L-1
则A∶B=10-4
方法2(巧解法):NaOH(aq)中,水的电离被抑制;CH3COONa(aq)中,水的电离被促进;故A<B。
本题难度:一般
2、选择题 下列溶液中各离子的浓度关系不正确的是( )
A.0.1 mol・L-1CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)=0.1 mol・L-1
B.浓度均为0.1 mol・L-1 Na2CO3溶液和稀盐酸等体积混合后的溶液中:
c(CO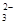 )+c(OH-)=c(H+)+c(H2CO3)
)+c(OH-)=c(H+)+c(H2CO3)
C.25 ℃时,pH=9.4、浓度均为0.1 mol・L-1的HCN与NaCN的混合溶液中:
c(Na+>c(CN-)>c(HCN)>c(OH-)
D. 3.0 L 0.1 mol・L-1 NaOH溶液中缓慢通入CO2至溶液增重8.8 g时,溶液中:
c(Na+)>c(CO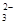 )>c(HCO
)>c(HCO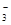 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
参考答案:CD
本题解析:A、物料守恒,正确;B、混合得到NaHCO3,质子守恒,正确;C、此混合溶液中存在HCN电离平衡和NaCN水解平衡,溶液为碱性,以水解平衡为主,故c(HCN)>c(Na+>c(CN-)> c(OH-),错误;
D、0.3mol NaOH通入0.2mol CO2,产物为同浓度的Na2CO3和NaHCO3,其中存在水解和电离平衡,其中以Na2CO3第一步水解为主,故有c(Na+)> c(HCO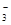 )>c(CO
)>c(CO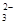 )> c(OH-)>c(H+),错误。
)> c(OH-)>c(H+),错误。
本题难度:一般
3、填空题 (14分)(1)常温时,将浓度为m mol・ L-1的CH3COOH溶液和n mol・L-1NaOH溶液等体积混合,混合后溶液的pH=7,m与n的大小关系是m?n(填“>”、“<”或“=”,下同);若将PH=2的CH3COOH溶液和PH=12的NaOH溶液等体积混合,混合溶液的PH?7
(2)消防用的泡沫灭火器内装的药品是硫酸铝溶液和碳酸氢钠溶液,用离子方程式表示二者混合时发生的反应?
(3)常温下某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱溶液混合pH=7,则酸溶液体积V1和碱溶液体积V2的关系为?
(4)常温时KSP[Cu(OH)2]= 2.2×10-20,将Cu(OH)2溶于2.2mol/LCuCl2溶液中形成平衡,溶解平衡方程式为?,溶液的PH为?
(5)物质的量浓度相同的下列溶液①(NH4)2CO3 ?②(NH4)2SO4 ?③NH4HCO3?④NH4HSO4?⑤NH4Cl?
⑥NH3・H2O。c(NH4+)由小到大的排列顺序是?(填序号)
参考答案:⑴m > n;混合溶液的PH<7;?⑵Al3++3HCO3-=Al(OH)3↓+3CO2↑
⑶V2=100V1?或 (V1∶V2=1∶100)?⑷Cu(OH)2(s) Cu2+(aq)+2OH-(aq), pH =" 4" ;?
Cu2+(aq)+2OH-(aq), pH =" 4" ;?
⑸c(NH4+)由小到大的排列顺序是 ⑥<③<⑤<④<①<②
本题解析:(1)由于CH3COOH是弱酸,而NaOH是强碱,若二者等体积混合,混合后溶液的pH=7,则必须是酸要过量一些。因此m>n。若将PH=2的CH3COOH溶液,c(H+)=10-2mol/L;由于醋酸是弱酸,所以c(HAc)> 10-2mol/L, PH=12的NaOH溶液,c(OH-)=10-2mol/L;NaOH是强碱,c(NaOH)= c(OH-)=10-2mol/L,若二者等体积混合,由于酸过量所以混合溶液的PH<7。(2)硫酸铝溶液和碳酸氢钠溶液反应的两种方程式是:Al3++3HCO3-=Al(OH)3↓+3CO2↑;(3)常温下某强酸溶液pH=a,c(H+)=10-amol/L;强碱溶液pH=b,c(OH-)=10-14÷10-b=10-(14-b),已知a+b=12,酸碱溶液混合pH=7,V1×10-a = V2・10-(14-b). V1: V2=10-(14-b: 10-a=10-2=1:100。(4) Cu(OH)2难溶于水。但是物质再难溶解,也存在一定的溶解度,在溶液中存在沉淀溶解平衡。Cu(OH)2的沉淀溶解平衡方程式是Cu(OH)2(s) Cu2+(aq)+2OH-(aq) ;c(Cu2+) ="2.2mol/L." KSP[Cu(OH)2]= c(Cu2+)・c2(OH-)= 2.2×10-20,所以c2(OH-)= 2.2×10-20÷2.2=1.0×10-20。因此c(OH-) =1.0×10-10。C(H+)=10-4mol/L。所以pH=4。(5)①(NH4)2CO3和②(NH4)2SO4每个物质能电离产生2个NH4+;而③NH4HCO3、④NH4HSO4、⑤NH4Cl 每种只能电离产生1个NH4+;因此c(NH4+)①和②一定大于③④⑤的。②(NH4)2SO4中只有NH4+离子水解,要消耗;①(NH4)2CO3中铵根离子水解使溶液显酸性,CO32-水解使溶液显碱性,二者相互促进,使NH4+的水解程度比②的小。即c(NH4+):①<②;⑤在NH4Cl中NH4+的水解使溶液显酸性,铵根离子水解消耗;④NH4HSO4电离方程式是:NH4HSO4= NH4++H++ SO42-。电离产生的H+对NH4+的水解起抑制作用,使铵根离子的浓度比⑤大,即⑤<④。③NH4HCO3电离产生的离子都发生水解反应,水解相互促进,所以消耗的铵根离子较多,因此铵根离子的浓度比⑤小。⑥NH3・H2O是弱电解质,电离产生的两种浓度原小于盐电离产生的铵根离子的浓度。因此c(NH4+)由小到大的排列顺序是 ⑥<③<⑤<④<①<②
Cu2+(aq)+2OH-(aq) ;c(Cu2+) ="2.2mol/L." KSP[Cu(OH)2]= c(Cu2+)・c2(OH-)= 2.2×10-20,所以c2(OH-)= 2.2×10-20÷2.2=1.0×10-20。因此c(OH-) =1.0×10-10。C(H+)=10-4mol/L。所以pH=4。(5)①(NH4)2CO3和②(NH4)2SO4每个物质能电离产生2个NH4+;而③NH4HCO3、④NH4HSO4、⑤NH4Cl 每种只能电离产生1个NH4+;因此c(NH4+)①和②一定大于③④⑤的。②(NH4)2SO4中只有NH4+离子水解,要消耗;①(NH4)2CO3中铵根离子水解使溶液显酸性,CO32-水解使溶液显碱性,二者相互促进,使NH4+的水解程度比②的小。即c(NH4+):①<②;⑤在NH4Cl中NH4+的水解使溶液显酸性,铵根离子水解消耗;④NH4HSO4电离方程式是:NH4HSO4= NH4++H++ SO42-。电离产生的H+对NH4+的水解起抑制作用,使铵根离子的浓度比⑤大,即⑤<④。③NH4HCO3电离产生的离子都发生水解反应,水解相互促进,所以消耗的铵根离子较多,因此铵根离子的浓度比⑤小。⑥NH3・H2O是弱电解质,电离产生的两种浓度原小于盐电离产生的铵根离子的浓度。因此c(NH4+)由小到大的排列顺序是 ⑥<③<⑤<④<①<②
本题难度:一般
4、选择题 若以w1和w2分别表示浓度为a mol・L-1和b mol・L-1氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小)
[? ]
A.2w1=w2
B.2w2=w1
C.w2>2w1
D.w1<w2<2w1?
参考答案:C
本题解析:
本题难度:一般
5、选择题
A.自来水
B.0.5 mol・L-1盐酸
C.0.5 mol・L-1 CH3COOH溶液
D.0.5 mol・L-1 KCl溶液
参考答案:B
本题解析:溶液混合后导电能力变化的大小,关键看混合后溶液中自由移动离子的浓度的变化。由于自来水几乎不导电,加入0.05 mol NaOH后,导电性突然增大;醋酸是弱电解质,加入NaOH后,生成强电解质CH3COONa,导电性明显增强;0.5 mol・L-1的KCl中加入0.05 mol NaOH固体后,离子浓度增大,导电能力增强;只有0.5 mol・L-1的盐酸,能与NaOH反应生成强电解质NaCl,不影响导电性。
本题难度:简单