ʱ��:2017-07-18 01:55:16
1��ѡ���� 2009��10��1�գ����찲�Ź㳡�Ͼ�����¡�صĹ����ı���ʽ��չ�����ҹ�ǿ����ۺϹ�������֮��̹�˵�չʾ������һ��������㣮һ���̹�˵IJ��ϴ����˸��ֽ����ĺϽ�����������ʮ����Ҫ��һ�֣���ô���й������ĸ���˵������ȷ����
A.����26��Ԫ�أ�λ��Ԫ�����ڱ��������ڣ���VIIIB��
B.�����������£�����������������Ӧ
C.�̷���������ھ�ˮ�����������仹ԭ��
D.FeO��HNO3��Ӧ���к���ɫ����ų�
�ο��𰸣�B
���������������A��Feλ�����ڱ��������ڣ���VIII�壻
B��Fe����Fe3+��Ӧ��
C���̷����ھ�ˮ�������������ԣ�
D��FeO��ŨHNO3��Ӧʱ���к���ɫ����ų���
���A��Feλ�����ڱ��������ڣ���VIII�壬��A����
B�������������£������������ᷴӦ����Fe3+��Fe����Fe3+��Ӧ����Fe2+����B��ȷ��
C���̷���������ھ�ˮ��������Fe2+��ˮ����������Ƶ�Fe��OH��3���壬�����˽���������ԣ����̷��������ܾ�ˮ����C����
D��FeO��ŨHNO3��Ӧʱ���к���ɫ����ų�����ϡ���ᷴӦ����NO����ɫ����D����
��ѡB��
���������⿼�������йػ���������ʺ���;����Ŀ�Ѷ��еȣ�����ע�������ػ���֪ʶ�Ļ��ۣ�
�����Ѷȣ�����
2��ѡ���� ��a g�����������Ļ������������������г�ַ�Ӧ������ʣ�࣬��òμӷ�Ӧ��HClΪ0��08 mol���ų���״���µ�����0��224 L���������ж�����ȷ����
A��ԭ�������n��Fe����n��Fe2O3����2��1
B������Һ�е���KSCN��Һ����Ѫ��ɫ
C��������ԭ����������
D����ʱ��Һ��Fe2����Fe3�������ʵ���֮��Ϊ3��1
�ο��𰸣�A
�����������״���µ�����0��224 LΪ���������ʵ���Ϊ0.01mol����Ӧ������ת�Ƶĵ������ʵ���Ϊ0.02mol����������HCL��Ӧ�����ʵ���Ϊ0.01mol����ӦʱҪ����HCL�����ʵ���Ϊ0.02mol�����ڷ�Ӧ��HCL�����ʵ���Ϊ0��08 mol�����Կɵ������������ʵ���Ϊ0.01mol������������ǿ����ϵΪ ����������������HCL���ɵ��Ȼ�������������Ӧ����
����������������HCL���ɵ��Ȼ�������������Ӧ���� ���������������ʵ���Ϊ0.01mol������
���������������ʵ���Ϊ0.01mol������
A��ȷ��B������Ӧ����Һ���� ��C���������������������ʵ����ɼ����ԭ������������D������Һ����
��C���������������������ʵ����ɼ����ԭ������������D������Һ����
�����Ѷȣ�һ��
3������� ��ҵ����ij����������Cu2O��Al2O3��Fe2O3��SiO2����ȡͭ�IJ����������£�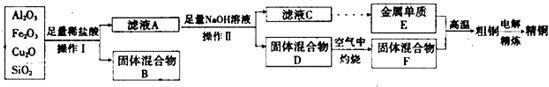
��֪��Cu2O+2H+�TCu+Cu2++H2O
��1��ʵ�����I������Ϊ?���ڿ��������չ�������Dʱ���õ����ֹ������ʵ������������������ƾ��ơ��������⣬����?�����������ƣ���
��2����ҺA����Ԫ�صĴ�����ʽΪ?�������ӷ��ţ������ɸ����ӵ����ӷ���ʽΪ?��������ҺA�д��ڸ����ӵ��Լ�Ϊ?�����Լ����ƣ���
��3������E�����F������ijһ��Ӧ�����ں��Ӹֹ죬�÷�Ӧ�Ļ�ѧ����ʽΪ?��
��4�������£���pH��NaAlO2��NaOH������Һ�У���ˮ�������c��OH-��ǰ��Ϊ���ߵ�108������������Һ��pH=?��
��5�������õ�ⷨ���д�ͭ����ʱ������������ȷ����?������ţ���
a������ȫ��ת��Ϊ��ѧ��
b����ͭ�ӵ�Դ����������������Ӧ
c����ͭ��������������Һ��Cu2+Ũ�ȼ�С
d����ͭ����ʱͨ���ĵ�������������ͭ������ȷ����ϵ
�ڴ�Ũ���ᡢŨ���ᡢ����ˮ��ѡ�ú��ʵ��Լ����ⶨ��ͭ��Ʒ�н���ͭ�������������漰����Ҫ����Ϊ����ȡһ����������Ʒ��?�����ˡ�ϴ�ӡ����������ʣ�����ͭ������������ȱ�ٵIJ������裬���������������̵�ϸ�ڣ�
�ο��𰸣�
���������
�����Ѷȣ�һ��
4��ʵ���� ��16�֣�ͭ��Ũ���ᷴӦ��ʵ��װ����ͼ��ʾ��
��1�� װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ��?����Ӧ�������Թ�B�е�������?���Թ�C��������?��
��2�� ����D���¶�(���߶�)Ӧλ��?��Һ���ϡ�Һ���£�������D�������У���ʵ��������ų�װ���е�SO2����?��
ʵ���з����Թ��ڳ��˲�����ɫ�����⣬��ͭ˿���滹�к�ɫ��������ɣ����п��ܺ���CuO��Cu2O��CuS��Cu2S��Ϊ̽���ijɷ֣����������µ�ʵ�顣
�������Ͽ�֪��Cu2O + 2HCl =CuCl2+ Cu + H2O�� 2Cu2O + O2���� 4CuO��2CuS+3O2����2CuO+2SO2��Cu2S+2O2����2CuO+SO2��CuS�� Cu2S��ϡHCl����Ӧ��
 ��3�� �������ڿ���������ʱ��ʹ�õ�ʵ���������˲����������żܡ��ƾ����⣬�������У�?��
��3�� �������ڿ���������ʱ��ʹ�õ�ʵ���������˲����������żܡ��ƾ����⣬�������У�?���ο��𰸣�33.��16�֣���1��Cu +2H2SO4(Ũ) ��CuSO4+SO2��+2H2O (2��)��Ʒ����Һ��ɫ��2�֣������ն����SO2����ֹ��Ⱦ������2�֣�
��2��Һ���£������� (4��)
��3�������ǡ�����������ǯ����2�֣�����ǯ��д���۷֣�
��4��2Cu+O2��2CuO (2��)
��5��CuS��2�֣�
��������� ��1�� ��ʵ���о�����ͭ��Ũ����ķ�Ӧ�������Aװ���з����ķ�Ӧ����ʽΪCu +2H2SO4(Ũ) ��CuSO4+SO2��+2H2O����Ӧ����SO2���ɣ����B�е�Ʒ����Һ��Ư����ɫ��C�Թ������չ���SO2��Ŀ�ģ���ֹSO2��Ⱦ������
��2�� ����Aװ�����Ʊ�SO2�ķ���װ�ã����Ե���D���¶˱��������Һ�У����ܷ�ֹ������SO2����ӵ���D���ݳ�����������D����������ʵ������������ų�Aװ�õ�SO2��ͬʱ�ܹ�ƽ��A��B����ѹ����ֹB��Һ�嵹��������������ǰ�D�¶˴���Һ������
��3�� ���յ�ʵ���þ߱���ʹ�����µ�������������������ʹ�õĻ��������ǡ�����ǯ�ȡ�
��4���������е��жϣ��ù��������CuO��Cu2O��CuS��Cu2S�������ϡ�����ܽ⣬������֪�ķ�Ӧ����Ӧ�õ��Ĺ����ҿ�����Cu��CuS��Cu2S���Թ����ҽ������գ���˳�����֪�ļ������շ�Ӧ�⣬�����ܷ����ķ�ӦΪ����ͭ������2Cu+O2��2CuO��
��5�� ���ݣ�4���ķ��������÷�Ӧ�ķ���ʽ�Ը��ֳɷ����ս�������ƶϷ�������Cu���գ���������CuOʹ�������أ���CuS���գ����ղ���CuOʹ������С����Cu2S���գ���������CuO���������䡣���Ҫ��������������ǰ��������С��������б��뻹������ʹ����ǰ��������С��CuS��
�����Ѷȣ�һ��
5��ѡ���� ������������������������ϡ�����ϡ���ᣬ�ֱ�����������������Ӧ��������˳��õ��������������ǣ���
A 1:1��?B 1:3 ?C 98:73 ?D 73:49
�ο��𰸣�C
���������������������˵������ȫ��Ӧ��ѧ�������ײ�����1��ѡA���������������ʵIJ�ͬ��������������������������ϡ�����ϡ���ᣬ˵�����к��е�����HCl��H2SO4��������ȵģ�HCl��H2SO4����ȫ��Ӧ����������������������Ӧ����HCl��H2SO4��������Ԫ�ص������ȡ���������HCl��H2SO4������Ϊm����������n����õ�������������Ϊ��2��m��n��36.5 ��2��m��n��98 ="?" 98 : 73��
�����Ѷȣ���