ʱ��:2017-07-18 01:18:24
1������� (15 ��)��������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷Ͼɵ�ص�ͭñ(Cu��Zn �ܺ���ԼΪ99%)����Cu���Ʊ�ZnO �IJ���ʵ��������£�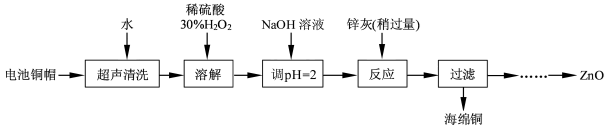
(1)��ͭñ�ܽ�ʱ����H2O2��Ŀ����?(�û�ѧ����ʽ��ʾ)����ͭñ�ܽ���ȫ�� �轫��Һ�й�����H2O2��ȥ����ȥH2O2�ļ�㷽����?��
(2)Ϊȷ������п��(��Ҫ�ɷ�ΪZn��ZnO������Ϊ������������)������ʵ������ⶨ��ȥH2O2����Һ��Cu2���ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2������Һ�ڴ�����ƿ 91ExAm.org�У�������ˮϡ�ͣ�������ҺpH=3~4�����������KI����Na2S2O3����Һ�ζ����յ㡣���������з�Ӧ�����ӷ���ʽ���£�ҡҡ2Cu2��+4I��=2CuI(��ɫ)��+I2? 2S2O32�� +I2=2I��+S4O62��
�ٵζ�ѡ�õ�ָʾ��Ϊ?���ζ��յ�۲쵽������Ϊ?��
�����ζ�ǰ��Һ�е�H2O2û�г��������ⶨ��Cu2����������?(�ƫ�ߡ�����ƫ�͡����䡱)��
(3)��֪pH>11 ʱZn(OH)2������NaOH��Һ����[Zn(OH)4]2-���±��г��˼������������������������pH(��ʼ������pH ����������Ũ��Ϊ1. 0 mol��L-1����)��
| ? | ��ʼ������pH | ������ȫ��pH |
| Fe3�� | 1. 1 | 3. 2 |
| Fe2�� | 5. 8 | 8. 8 |
| Zn2�� | 5. 9 | 8. 9 |
�ο��𰸣�(1)��Cu+H2O2+H2SO4=CuSO4+2H2O?�ڼ���(����)
(2)�ٵ�����Һ?��ɫ��ȥ?��ƫ��
(3)������Һ�м�������30% H2O2��ʹ���ַ�Ӧ
�ڵμ�1.0 mol��L-1NaOH��������ҺpH ԼΪ5(��3.2��pH<5.9)��ʹFe3��������ȫ
����Һ�еμ�1. 0 mol��L-1NaOH��������ҺpH ԼΪ10(��8. 9��pH��11)��ʹZn2��������ȫ
�����������1��Ŀ�귴Ӧ������֪��������Ӧ��ӵõ�����Ӧ��Ҳ�ж�Ӧ������ã��÷�Ӧ�����ڸ��ֽ���ε�ˮ�⣬�����ɵ������Ǽ��飻
��2��ϡ������������Ƿ�Ӧ�һ��������������ֹ�����������������ļ��������Ϊԭ��������д洢����ȫ���ų�������������������ᷴӦҲ������������ɼ��������52molH2������Al������ǿ�Ƚϵͣ����������˷�Ӧ������������Ҫ�������������ʡ�
��3�����Ǹ����Dz��ϣ����븺����Ӧ����ʧȥ���Ӳ�����������������ӷ�Ӧ����ƫ��������ӣ������������õ�������������
�����㶨λ���ϵ����ͭ�Ļ��ա�ZnO���Ʊ�ʵ��
�����Ѷȣ�һ��
2��ѡ���� �������������������ϡ�����У����ܷ����ķ�Ӧ�ǣ�?��
A��ֻ���û���Ӧ
B��ֻ�и��ֽⷴӦ
C���û����ֽⷴӦ
D���û��ͷֽⷴӦ
�ο��𰸣�C
����������������������ϡ�����У����DZ�����������������������ᷴӦ�����Ȼ�����ˮ����ʱ��Һ�ʻ�ɫ����������ȫ��Ӧ������ϡ����Ӵ�������Ӧ�������Ȼ��������������䷽��ʽΪ��6HCl+Fe2O3�T2FeCl3+3H2O�����ֽⷴӦ����2HCl+Fe�TFeCl2+H2�����û���Ӧ����
�����Ѷȣ�һ��
3��ѡ���� ���������ڳ����¿�����������ʢ�ŵ���
A��������
B��Ũ����
C��Ũ����
D��������Һ
�ο��𰸣�B
�����������
�����Ѷȣ���
4������� ij��ѧ��ȤС��������ʯ����Ҫ�ɷ�ΪFe2O3������Si O2��A12O3�����ʣ���ȡFe2O3�������ֳ����£�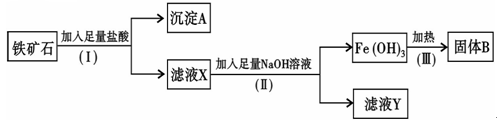
��1����I���ͣ������з�����Һ�ͳ����IJ���������?��
��2������A����Ҫ����? ?���ѧʽ��������B��?���ѧʽ����
?���ѧʽ��������B��?���ѧʽ����
��3����ҺY�е������ӳ�OH-��Cl-�⣬����?���ѧʽ����
��4��д��������������Fe(OH)3�����ӷ���ʽ?
�ο��𰸣���6�֣�
(1������?
(2)? SiO2?Fe2O3
(3��A1O2-
(4)Fe3++3OH-? ?Fe(OH)3��
?Fe(OH)3��
�����������
�����Ѷȣ�һ��
5��ѡ���� ���л������У������ɻ��Ϸ�Ӧ�Ƶõ��ǣ�������
A��Fe��OH��3
B��FeCl2
C��Fe��OH��2
D��FeCl3
�ο��𰸣�C
���������
�����Ѷȣ�һ��