时间:2017-07-18 00:38:16
1、选择题 已知C(金刚石) C(石墨)ΔH =" -" Q(Q>0),下列热化学方程式放出热量最多的是
C(石墨)ΔH =" -" Q(Q>0),下列热化学方程式放出热量最多的是
A.C(金刚石)+ O2(g)=CO(g)ΔH =" -" Q1
O2(g)=CO(g)ΔH =" -" Q1
B.C(石墨)+  O2(g)="CO(g)" ΔH =" -" Q2
O2(g)="CO(g)" ΔH =" -" Q2
C.C(金刚石) + O2(g)=CO2(g) ΔH =" -" Q3
D.C(石墨)+ O2(g)=CO2(g) ΔH =" -" Q4
参考答案:C
本题解析:从已知反应C(金刚石)=C(石墨)的△H<0可知,金刚石的能量比石墨高,△H=生成物能量-反应物能量,反应物能量比生成物能量高的越多,放热越多,金刚石和石墨相比,金刚石燃烧放热比石墨多,又相同物质的量的金刚石,完全燃烧生成二氧化碳比生成CO放出的热量多,故C正确,故选:C.
考点:反应热和焓变
本题难度:一般
2、填空题 (12分)红磷P(s)和Cl2(g)发生反应生成 PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。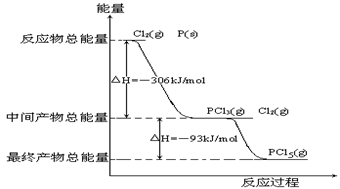
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式______________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________ ____
(3)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
参考答案: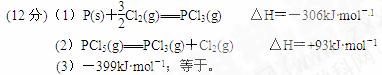
本题解析:略
本题难度:一般
3、选择题 为了测定酸碱反应的中和热,计算时至少需要的数据是
①酸的浓度和体积;②碱的浓度和体积;③比热容;④反应后溶液的质量;⑤生成水的物质的量;⑥反应前后的温度变化;⑦操作所需时间;
A.①②③⑥⑦
B.①③④⑤
C.③④⑤⑥
D.①②③④⑤⑥
参考答案:C
本题解析:中和热是指在一定条件下,强酸强碱的稀溶液中,酸与碱反应生成1mol水时所放出的热量,所以根据△H=[(m1+m2)×c×(T2-T1)]÷n(H2O),需要测量的数据应该是③④⑤⑥,选C。
考点:考查中和热的测定。
本题难度:一般
4、选择题 中心原子采取sp2杂化的是? ( )
A.NH3
B.BCl3
C.PCl3
D.H2O
参考答案:B
本题解析:根据杂化轨道数判断杂化类型,杂化轨道数=δ键数+孤对电子对数,则A、N原子杂化轨道数=δ键数+孤对电子对数=3+1=4,所以采取sp3杂化,故错误;B、B原子杂化轨道数=δ键数+孤对电子对数=3+0=3,所以采取sp2杂化,故正确;C、P原子杂化轨道数=δ键数+孤对电子对数=3+1=4,所以采取sp3杂化,故错误;D、O原子杂化轨道数=δ键数+孤对电子对数=2+2=4,所以采取sp3杂化,故错误,答案选C。
本题难度:一般
5、选择题 下列各分子中,所有原子都满足最外层为8电子结构的是( )
A.HCl
B.PCl3
C.PCl5
D.CH4
参考答案:A、HCl中Cl原子最外层电子为7+1=8,H原子的最外层电子数=1+1=2,故A错误;
B.PCl3中,P原子的最外层电子为:5+3=8,Cl原子的最外层电子为:7+|-1|=8,都满足8电子稳定结构,故B正确;
C.PCl5中,P原子的最外层电子为:5+5=10,Cl原子的最外层电子为:7+|-1|=8,不都满足8电子稳定结构,故C错误;
D、CH4中,C原子的最外层电子数为4+4=8,H原子的最外层电子数=1+1=2,故D错误.
故选B.
本题解析:
本题难度:简单