时间:2017-07-18 00:31:17
1、选择题 常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液,有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)。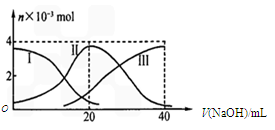
根据图示判断,下列说法正确的是
A.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.等体积等浓度的NaOH溶液与H2A溶液混合,其溶液中水的电离程度比纯水的大
C.向Na2A溶液加入水的过程中,pH可能增大也可能减小
D.NaHA溶液中:c(OH-)+c(A2-) = c(H+)+c(H2A)?
参考答案:AD
本题解析:A、此时物质恰好反应生成NaHA,图中读出c(HA-)>c(A2-)> c(H2A)知NaHA电离大于水解,以电离为主,故有c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),正确;B、此时同A选项,NaHA电离溶液为酸性抑制水的电离,错误;C、Na2A溶液水解呈碱性,加水稀释离子浓度减少,pH减小,错误;D、质子守恒,正确。
本题难度:一般
2、选择题 相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
[? ]
A.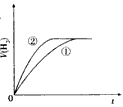
B.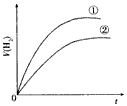
C.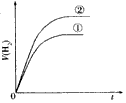
D.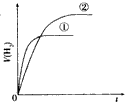
参考答案:C
本题解析:
本题难度:一般
3、填空题 NaHCO3在水溶液中,HCO3-的电离程度小于HCO3-的水解程度。回答下列有关问题:
⑴H2CO3的电离方程式为 ;
⑵NaHCO3溶液显碱性,原因是(用离子方程式表示)
;
⑶在该溶液中,c(Na+)、c(H+)、c(HCO3-)、c(OH-)的大小关系为
;
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)= ;
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)= 。
参考答案:⑴H2CO3 H++HCO3-, HCO3- H++CO32-; ⑵HCO3-+H2O H2CO3+OH-; ⑶c(Na+)>c(HCO3-)>c(OH-)>c(H+);
⑵HCO3-+H2O H2CO3+OH-; ⑶c(Na+)>c(HCO3-)>c(OH-)>c(H+);
⑷c(HCO3-)+c(OH-)+2c(CO32-); ⑸c(HCO3-)+c(H2CO3)+c(CO32-)(各1分)
本题解析:略
本题难度:一般
4、选择题 已知某温度下,Ka (HCN)= 6.2×10-10 mol・L-1、Ka (HF)=" 6.8×10" - 4 mol・L-1、Ka (CH3COOH)= 1.8×10-5 mol・L-1、Ka (HNO2)=" 6.4×10" - 6 mol・L-1。物质的量浓度都为0.1 mol・L-1的下列溶液中,pH最小的是
A.HCN溶液
B.HF溶液
C.CH3COOH溶液
D.HNO2溶液
参考答案:B
本题解析:针对四种一元弱酸来讲,当物质的量浓度相等时,电离常数Ka越大,酸性相对越强,pH越小,故答案为B
本题难度:一般
5、选择题 醋酸是一种常见的弱酸,为了证明醋酸是弱电解质,某同学开展了题为“醋酸是弱电解质的实验研究”的探究活动。他设计了如下方案,其中错误的是
[? ]
A.先配制一定量的0. 10mol/L的CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸是弱电解质
B.先配制一定量0. 01mol/L和0.1mol/L的CH3COOH溶液,分别用pH计测它们的pH,若两者pH相差小于1个单位,则可证明醋酸是弱电解质
C.先测0.10mol/L CH3COOH溶液的pH,然后将其加热至100℃,再测pH,如果pH变小,则可证明醋酸是弱电解质
D.配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质
参考答案:C
本题解析:
本题难度:一般