时间:2017-07-18 00:27:59
1、选择题 将50 mL0.1 mol・L-1NaCl和50 mL0.5 mol・L-1CaCl2溶液混合后,若溶液的体积为二者体积之和,则混合溶液中c(Cl-)为
A.1 mol・L-1
B.0.55 mol・L-1
C.0.67 mol・L-1
D.2 mol・L-1
参考答案:B
本题解析:
本题难度:一般
2、选择题 0.5mol Na2SO4中含有Na+数目是
A.3.01x1023
B.6.02x1023
C.0.5
D.1
参考答案:B
本题解析:试题分析:0.5mol Na2SO4中钠离子的物质的量为0.5mol×2=1mol,
则由N=n×NA可知,
则钠离子的个数为1mol×NAmol-1=NA≈6.02×1023,
故选B。
考点:阿伏加德罗常数 电解质在水溶液中的电离
点评:有关阿伏伽德罗常数的计算,题目在注重对计算关系的考查的同时,又隐含对物质状态、物质结构、氧化还原反应、电离、水解知识的考查。
本题难度:一般
3、选择题 下列实验装置不适用于物质分离的是
[? ]
A.
B.
C.
D.
参考答案:D
本题解析:
本题难度:简单
4、选择题 化学工作者从反应RH+Cl2(气)→RCl(液)+HCl(气)受到启发,提出在制取农药和有机合成中可获得盐酸,此设想已成为事实。请指出从上述反应物中得到盐酸的最佳方法?(?)
A.蒸馏法
B.水洗分液法
C.升华法
D.有机溶剂萃取法
参考答案:B
本题解析:蒸馏法是分离沸点不同的两种液体的方法。升华法分离熔点不同的两种固体的方法。水洗分液法是利用HCl极易溶于水而RCl难溶于水,萃取分理出盐酸。
本题难度:一般
5、简答题 (2012?天津)完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
A.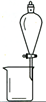
用CCl4提取溴水中的Br2
B.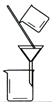
除去乙醇中的苯酚
C.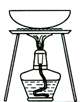
从KI和I2的固体混合物中回收I2
D.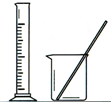
配制100mL 0.1000mol?L-1 K2Cr2O7溶液
参考答案:A.溴单质易溶于四氯化碳,且四氯化碳与水互不相溶,故A正确;
B.苯酚易溶于乙醇,不分层,不能用分液漏斗分离,故B错误;
C.加热后,碘单质易升华,剩余的是KI,故C错误;
D.烧杯用来粗略配制溶液,无法精确到0.0001,故D错误.
故选A.
本题解析:
本题难度:一般