时间:2017-07-17 23:42:46
1、选择题 下列关于原电池的叙述中正确的是( )
A.原电池能将化学能转变为电能
B.原电池负极发生的电极反应是还原反应
C.原电池在工作时其正极不断产生电子并经外电路流向负极
D.原电池的电极只能由两种不同的金属构成
2、选择题 镁―H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是
A.电池总反应为Mg+H2O2 = Mg(OH)2
B.正极发生的电极反应为H2O2+2H++2e- = 2H2O
C.工作时,正极周围海水的pH减小
D.电池工作时,溶液中的H+向负极移动
3、选择题 海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4A1+3O2+6H2O=4A1(OH)3,下列说法错误的是(?)
A.该装置能实现化学能转化为电能
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面
D.该电池通常只需更换铝板就可继续使用
4、选择题 结合下图判断,下列叙述正确的是?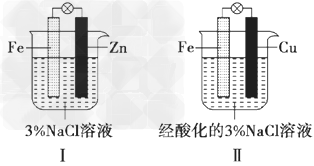
[? ]
A.?I和II中正极均被保护
B.?I和II中负极反应均是Fe-2e-=Fe2+
C.?I和II中正极反应均是O2+2H2O+4e-=4OH-
D.?I和II中分别加入少量KSCN和氯水溶液,溶液均变为血红色
5、计算题 研究碳及其化合物的性质对促进低碳社会的构建具有重要意义。
(1)将不同量的CO(g)和H2O(g)分别通人体积为2L的恒容密闭容器中,进行反应 CO(g)+H2O(g) CO2(g)+H2(g),得到如下两组数据:
CO2(g)+H2(g),得到如下两组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |