时间:2017-07-10 20:37:06
1、填空题 下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 2 ① ② ③ 3 ④ ⑤ ⑥ ⑦ ⑧ 4 ⑨ |
参考答案:根据元素在周期表中的分布,可以推知①是C,②是N,③是O,④是Na,⑤是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K.
(1)在这些元素中,化学性质最稳定的是稀有气体Ar,故答案为:Ar;
(2)根据元素周期律:同周期元素的原子,从左到右最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱,同主族元素的原子,从下到上最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱可以推知酸性最强的式是高氯酸,碱性最强的是KOH,故答案为:HClO4;KOH;
(3)氢氧化铝是两性氢氧化物,所以最高价氧化物是两性氧化物的元素是Al,能和强碱反应生成盐和水,实质是:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al;Al(OH)3+OH-=AlO2-+2H2O;
(4)硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为: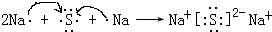
,故答案为: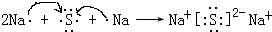
;离子;
(5)二氧化碳是碳原子和氧原子间通过极性共价键形成的共价化合物,电子式为: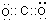
,故答案为: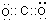
;极性.
本题解析:
本题难度:一般
2、选择题 如图为短周期的一部分,推断关于Y、Z、M的说法正确的是( )
A.非金属性:Y>Z>M
B.X为稀有气体元素
C.原子半径:M>Z>Y
D.Y原子的结构示意图可表示为: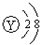
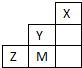
参考答案:由元素在周期表中的相对位置可知,X为氦元素,Y为F元素,Z为S元素,M为Cl元素.
A、同周期随原子序数增大,非金属性增强,所以非金属性M>Z,同主族自上而下非金属性减弱,所以非金属性Y>M,所以非金属性Y>M>Z,故A错误;
B、X为氦元素,属于稀有气体元素,故B正确;
C、同周期随核电荷数增大,原子半径减小,所以原子半径Z>M,同主族自上而下原子半径增大,所以原子半径M>Y,所以原子半径Z>M>Y,故C错误;
D、氟原子质子数为9,核外电子数为9,有2个电子层,最外层有7个电子,原子结构示意图为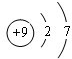
,故D错误.
故选:B.
本题解析:
本题难度:简单
3、选择题 下列结论不正确的是( )
A.微粒半径:S>S2->Cl->F
B.酸性:HClO4>H2SO4>H3PO4
C.氧化性:Cl2>S>Se>Te
D.离子还原性:S2->I->Br->OH-
参考答案:A、根据微粒半径大小比较的方法:电子层越多半径越大,所以F半径最小,电子层数一样,核电荷数越多半径越小,所以S2->Cl-,核电荷数一样,核外电子数越多,半径越大S<S2-,即S2->S>Cl->F,故A错误;
B、同周期从左到右,最高价氧化物对应水化物的酸的酸性逐渐增强,即HClO4>H2SO4>H3PO4,故B正确;
C、同周期从左到右单质的氧化性逐渐增强,所以氧化性:Cl2>S,同主族,从上到下,单质的氧化性逐渐减弱,所以S>Se>Te,即氧化性:Cl2>S>Se>Te,故C正确;
D、根据元素周期律,单质氧化性顺序是:Cl2>Br2>I2>S,所以离子还原性:S2->I->Br->OH-,故D正确.
故选A.
本题解析:
本题难度:简单
4、选择题 某元素的离子X2+有6个电子层,最外层有2个电子,将XO2溶于浓盐酸时,有黄绿色的气体产生,则下列相关说法正确的是?
[? ]
A.元素X位于周期表第六周期ⅣA族
B.元素X为ⅡA族元素
C.XO2具有强氧化性
D.X2+具有强还原性
参考答案:AC
本题解析:
本题难度:一般
5、选择题 下列实验现象、结论及其推理都正确的是?(?)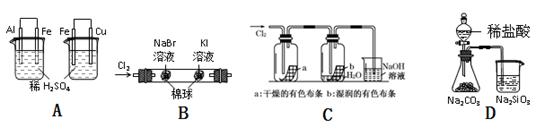
| 实验 | 实验现象 | 结论 |
| A | 左烧杯中铁不断溶解,右烧杯中铁表面有气泡 | 活动性:Al>Fe>Cu |
| B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | a中布条不褪色,b中布条褪色 | 干燥氯气无漂白性,潮湿的氯气有漂泊性 |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:S>C>Si |
参考答案:C
本题解析:略
本题难度:一般