时间:2017-07-10 20:27:50
1、选择题 已知:常温下氢氟酸Ka=3.5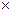 10-4 ,醋酸Ka=1.8
10-4 ,醋酸Ka=1.8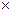 10-5,能正确描述在它们的钠盐溶液中,水电离出的c(H+)与盐浓度的关系曲线的是
10-5,能正确描述在它们的钠盐溶液中,水电离出的c(H+)与盐浓度的关系曲线的是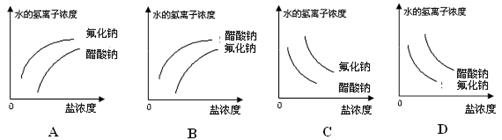
参考答案:B
本题解析:略
本题难度:一般
2、选择题 关于pH相同的醋酸和盐酸,下列叙述正确的是
A.取等体积的醋酸和盐酸,分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n
B.取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率:盐酸大于醋酸
C.取等体积的两种酸,分别用完全一样的NaOH溶液进行中和,醋酸消耗NaOH的物质的量比盐酸消耗的多
D.两种酸中c (CH3COO-) > c (Cl-)
参考答案:C
本题解析:盐酸是强酸,醋酸是弱酸,醋酸溶液中存在电离平衡,加水稀释能促进弱电解质电离,pH相同的醋酸和盐酸,醋酸的浓度大于盐酸,不同的酸和相同金属反应,生成氢气的速率与溶液中离子浓度成正比;A、pH相同、体积相同的醋酸和盐酸两种溶液分别加水稀释后,促进醋酸的电离,结果两溶液的pH仍然相同,所以醋酸稀释的倍数大,即m>n,错误;B、pH相同的醋酸和盐酸氢离子浓度相同,所以取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸等于醋酸,错误;C、pH相同、体积相同的醋酸和盐酸,醋酸的物质的量大于盐酸,所以醋酸消耗NaOH的物质的量比盐酸多,正确;D、pH相同的醋酸和盐酸氢离子浓度相同,则氢氧根离子浓度也相同,根据电荷守恒知c(CH3COO-)=c(Cl-),错误。
本题难度:一般
3、选择题 将标准状况下1.12L氨气溶于500mL水中配制成溶液,从中取出5mL,有关这5mL溶液的叙?述正确的是
A.溶液中c(NH4+)< c(OH―)
B.氨水的物质的量浓度为0.1 mol・L―1
C.溶液的pH>13
D.与5mL 0.1mol・L―1HCl溶液恰好完全中和
参考答案:A
本题解析:A、一水合氨电离出铵根和氢氧根离子,水也可电离出氢氧根离子,故溶液中c(NH4+)< c(OH―) ,正确;B、氨气溶于500 mL水中,不考虑溶液体积的变化时,氨水的物质的量浓度为0.1 mol・L―1,实际上溶液体积不是500 mL,错误;C、氨水是弱电解质,c(OH―)<0.1 mol・L―1,则pH<13,错误;D、氨水的物质的量浓度不等于0.1 mol・L―1与等体积的0.1mol・L―1HCl溶液不是恰好反应,错误。
本题难度:一般
4、选择题 甲、乙两烧杯中分别装有相同体积、相同pH的氨水和NaOH溶液,各加入10 mL 0.1mol・L-1 AlCl3溶液,两烧杯中都有沉淀生成。下列判断正确的是
[? ]
A.甲中沉淀一定比乙中的多
B.甲中沉淀可能比乙中的多
C.甲中沉淀一定比乙中的少
D.甲中和乙中的沉淀可能一样多
参考答案:BD
本题解析:
本题难度:一般
5、选择题 下列物质中能抑制水的电离且使溶液呈现出酸性的是( )
A.Na2CO3
B.Al2(SO4)3
C.K2SO4
D.H2SO4
参考答案:D
本题解析:
本题难度:一般