ʱ��:2017-07-10 19:45:40
1������� �״�����Ϊȼ�ϵ�ص�ԭ�ϡ���CH4��H2OΪԭ�ϣ�ͨ�����з�Ӧ���Ʊ��״���
��CH4��g����H2O��g��=CO��g����3H2��g��? ��H��206.0 kJ��mol��1
��CO��g����2H2��g����CH3OH��g��?��H����129.0 kJ��mol��1
��1��CH4��g����H2O��g����Ӧ����CH3OH��g����H2��g�����Ȼ�ѧ����ʽΪ______________________________________________________��
��2����1.0 mol CH4��2.0 mol H2O��g��ͨ���ݻ�Ϊ100 L�ķ�Ӧ�ң���һ�������·�����Ӧ�����һ����ѹǿ��CH4��ת�������¶ȵĹ�ϵ����ͼ��
�ټ���100 ��ʱ�ﵽƽ�������ʱ��Ϊ5 min������H2��ʾ�÷�Ӧ��ƽ����Ӧ����Ϊ________��
��100 ��ʱ��Ӧ���ƽ�ⳣ��Ϊ________��
��3����ѹǿΪ0.1 MPa���¶�Ϊ300 �������£���a mol CO��3a mol H2�Ļ�������ڴ��������·�����Ӧ�����ɼ״���ƽ����������ݻ�ѹ����ԭ���� �������������䣬��ƽ����ϵ������Ӱ����________������ĸ��ţ���
�������������䣬��ƽ����ϵ������Ӱ����________������ĸ��ţ���
A��c��H2������
B������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
C��CH3OH �����ʵ�������
D������ƽ��c��H2��/c��CH3OH����С
E��ƽ�ⳣ��K����
��4��д���״���������KOH��Һ��ȼ�ϵ�ظ����ĵ缫��Ӧʽ��__________________________________________________��
��5���״���ˮ�ʻ����һ������Ⱦ����һ�ֵ绯ѧ��������������Ⱦ����ԭ���ǣ�ͨ���Co2��������Co3����Ȼ����Co3������������ˮ�еļ״�������CO2��������ʵ��������ͼװ��ģ���������̣�
��д�������缫��Ӧʽ____________________________��
��д����ȥ�״������ӷ���ʽ__________________________________��
�ο��𰸣���1��CH4��g����H2O��g��=CH3OH��g����H2��g��? ��H��77.0 kJ��mol��1
��2����0.003 mol��L��1��min��1����2.25��10��4
��3��CD
��4��CH3OH��6e����8OH��=CO32-��6H2O
��5��Co2����e��=Co3����6Co3����CH3OH��H2O=CO2����6Co2����6H��
�����������1��д�Ȼ�ѧ����ʽ��ע��ۼ�״̬��Ŀ�귴Ӧ���ɷ�Ӧ����ӵõ����������Ӧ�ȡ���2���������ʺ�ƽ�ⳣ��ʱҪע���ݻ������������H2�����ʣ�
����һ��v��H2����3v��CH4����3�� ��0.003 mol��L��1��min��1��
��0.003 mol��L��1��min��1��
�����������ݡ�����ʽ��
��?������ ��CH4��g���� ��H2Og= CO��g����3H2��g��
n��ʼ��/mol������1.0���� ��2.0��������0������0
n���䣩/mol������0.5���� ��0.5��������0.5����1.5
n��ƽ��/mol������0.5���� ��1.5��������0.5����1.5
v��H2���� ��
�� ��0.003 mol����1��min��1
��0.003 mol����1��min��1
K�� ��
�� ��2.25��10��4
��2.25��10��4
��3�����ѹ��Ϊԭ����һ�룬��Ũ�ȱ�Ϊԭ����2����ƽ����ƶ��Ǹ����������Ĺ��̣�Ũ�ȱ�ԭƽ���A����ѹǿ�������淴Ӧ���ʾ�����B����ѹǿ����ƽ��������Ӧ�����ƶ���C��D��ȷ��ƽ�ⳣ��ֻ���¶��йأ�E����4�������ϼ״���Ӧ��KOHΪ����ʣ�����ΪCO32-����������д������5����������������Ӧ��Co2������Co3����Co3�����״�����������Co2����CO2��ע����Һ�����ԡ�
�����Ѷȣ�����
2��ѡ���� �Զ�ײ�Ϊ�缫������ͼװ���зֱ���������ͨ��CH3OH��O2��������Ӧ�������������ⶨ������������b��a��������������ȷ���� 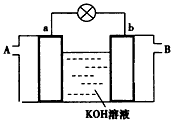
[? ]
A��A��ͨ��O2
B����Һ�е���������a���˶�
C�������ĵ缫��ӦΪ��2CH3OH+16OH--12e-=2CO32-+12H2O
D��b���Ǹ�ȼ�ϵ�صĸ���
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3������� ��̼������Ƭ��200mLϡH2SO4����������ɵ�ԭ����У�����̼���Ϲ��ų�3.36L����״��������ʱ�������������ٿˣ��ж��ٸ�����ͨ���˵��ߣ�
�ο��𰸣�����Ҫ������x��
��ԭ��صĵ�ط�ӦʽΪ��
? Fe+H2SO4=FeSO4+H2��
? 56g? 22.4L
? x?3.36L
����x=56g?��?3.36L22.4L=8.4g
��������8.4g��
��ת�Ƶ���y��
?Fe+H2SO4=FeSO4+H2�� ת�Ƶ���
?22.4L? 1.204��1023��
?3.36L? y
����y�T3.36L��1.204��1023��22.4L?=1.806��1023��
�ʴ�Ϊ��8.4g��1.806��1023����
���������
�����Ѷȣ�һ��
4��ѡ���� ����������ԭ�����ɵ�ط�Ӧ��ɵ���
A.�����ʵ�п������ȴ�п�����ᷴӦ���ʿ�
B.�����ڳ�ʪ�Ŀ�������ʴ
C.���������ᷴӦ������뼸������ͭ��Һ����ɼӿ췴Ӧ����
D.�������е�����¯��ʴ����
�ο��𰸣�D
���������
�����Ѷȣ���
5��ѡ���� ��ͼ��ʾ��������ָ�뷢��ƫת��X����֣�Y����ϸ��������������������(? )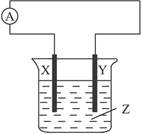
A��X��Cu,Y��Zn��Z��ϡH2SO4��Һ
B��X��Zn��Y��C��Z��CuSO4��Һ
C��X��Fe,Y��Cu,Z��Fe(NO3)3��Һ
D��X��Ag��Y��Zn,Z��AgNO3��Һ
�ο��𰸣�D
����������������֪X���Ǹ�ԭ��ص�������Y���Ǹ�����ֻ��Dѡ��������⡣
�����Ѷȣ���