时间:2017-07-10 19:14:37
1、选择题 在一定条件下KI、Zn、FeBr2分别与足量的Cl2反应,如果3个反应得失电子数目相等,则KI、Zn、FeBr2的物质的量之比为( )
A.1:2:3
B.3:2:1
C.6:3:2
D.2:3:6
2、选择题 下列是爱迪生电池分别在充电和放电时发生的反应:Fe+ NiO2+2H2O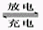 Fe(OH)2+Ni(OH)2,消耗0.54g H2O时,电解0.01molCuSO4和0.01molNaCl混合溶液100mL,两极产生气体标况下总体积是?
Fe(OH)2+Ni(OH)2,消耗0.54g H2O时,电解0.01molCuSO4和0.01molNaCl混合溶液100mL,两极产生气体标况下总体积是?
[? ]
3、填空题 (1)已知Fe3+的氧化性大于Cu2+,根据此性质,某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。用离子方程式表示其化学原理__________________
某实验小组对该厂生产印刷电路后所得的废液进行了分析: 取50.00 mL废液,向其中加入0.64 g金属铜,金属铜全部溶解;另取50. 00 mL废液,向其中加入足量的AgNO3溶液,析出沉淀43. 05 g。请回答以下问题:
(2)该厂产生的废液中所含金属离子有____ ;该厂原来使用的FeCl3溶液的物质的量浓度____ (反应前后溶液的体积变化忽略不计)。
4、简答题 已知H2S和?SO2?反应生成?S和?H2O
①写出反应的化学方程式并标出电子转移的方向和数目______
②上述反应中被氧化的硫原子和被还原的硫原子的物质的量之比为______
③现有H2S和?SO2混合气体1mol,充分反应后得到的产物中,若还原产物比氧化产物少1.6g,则反应中转移电子数为______NA,原混合物中H2S和?SO2的物质的量可能各是多少______.
5、选择题 24 mL浓度为0.05 mol/L的Na2SO3溶液恰好与20 mL 浓度为0.02mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
[? ]
A.+2
B.+3
C.+4
D.+5