时间:2017-07-10 18:39:29
1、选择题 25℃时,有c(CH3COOH)+c(CH3COO-)=" 0." 1 mol・L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是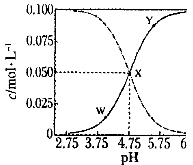
A.X点所表示的溶液中:c(Na+)+ c(OH-) = c(CH3COO-) + c(H+)
B.W 点所表示的溶液中:c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=" 0." 1mol・L-1
C.该温度下醋酸的电离平衡常数为10-4.75 mol・L-1
D.向X点所表示的溶液中加入等体积的0. 05mol・L-1NaOH溶液:c(H+)= c(CH3COOH)+c(OH-)
参考答案:C
本题解析:试题分析:A、根据图像可知,X点溶液显酸性,则根据电荷守恒可知c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),选项A不正确;B、W点溶液显酸性,同样根据电荷守恒可知 c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),所以c(Na+) +c(H+) 91exam.org-c(OH-) +c(CH3COOH)=2 c(CH3COOH)<0.1mol/L,B不正确;C、该温度下醋酸的电离平衡常数=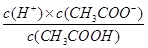 ,则根据X点的pH可知,该温度下醋酸的电离平衡常数为10-4.75 mol/L,选项C正确;D、向X点所表示的溶液中加入等体积的0. 05mol・L-1NaOH溶液,醋酸恰好反应生成醋酸钠,即溶液是醋酸钠溶液,所以根据质子守恒可知c(OH-)= c(CH3COOH)+ c(H+),D不正确,答案选C。
,则根据X点的pH可知,该温度下醋酸的电离平衡常数为10-4.75 mol/L,选项C正确;D、向X点所表示的溶液中加入等体积的0. 05mol・L-1NaOH溶液,醋酸恰好反应生成醋酸钠,即溶液是醋酸钠溶液,所以根据质子守恒可知c(OH-)= c(CH3COOH)+ c(H+),D不正确,答案选C。
考点:考查电离平衡常数的有关判断和计算、溶液中离子浓度大小比较
本题难度:一般
2、选择题 下列物质中,难溶于CCl4的是
[? ]
A.碘单质
B.水
C.苯
D.甲烷
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列物质在一定条件下能够与硫发生反应,且硫作还原剂的是
A.O2
B.Fe
C.H2
D.Zn
参考答案:A
本题解析:Fe、H2、Zn都是还原性物质,与硫反应时,硫作氧化剂.氧气具有强氧化性,与硫反应硫作还原剂.
本题难度:简单
4、选择题 在一支25 mL的酸式滴定管中盛入0.1 mol・L-1HCl溶液,其液面恰好在5 mL的刻度处,若滴定管中的溶液全部放入烧杯中,然后用0.1 mol・L-1NaOH溶液进行中和,则需NaOH溶液的体积( )
A.大于20 mL
B.小于20 mL
C.等于20 mL
D.等于5 mL
参考答案:A
本题解析:试题分析:因为盐酸液面恰好在5 mL的刻度处时,放出全部液体的体积要大于20 mL。因为HCl+NaOH===NaCl+H2O,所以消耗NaOH溶液的体积大于20 mL,即答案选A。
考点:考查滴定管构造
点评:该题是基础性试题的考查,也是高考中的常见题型。试题基础性强,侧重对学生基础知识的巩固和训练,难度不大。该题的关键是明确滴定管的构造特点。
本题难度:困难
5、选择题 将某溶液逐滴加入Fe(OH)3溶胶内,开始产生沉淀,继续滴加时沉淀又溶解,该溶液是
A.稀H2SO4溶液
B.稀NaOH溶液
C.稀MgSO4溶液
D.硅酸胶体
参考答案:A
本题解析:由于Fe(OH)3胶粒带有正电荷,故加电解质H2SO4、NaOH、MgSO4溶液均会引起胶体的聚沉.硅酸胶粒带负电荷,遇到带有正电荷的Fe(OH)3胶粒也会发生胶体的聚沉.当Fe(OH)3沉淀形成后,Fe(OH)3由于可与酸发生中和反应,故稀H2SO4溶液的加入,会使沉淀溶解.
本题难度:一般