时间:2017-07-10 18:32:00
1、选择题 室温下,某溶液中由水电离产生的c(H+)等于10-13 mol・L-1,该溶液的溶质不可能是( )
A.NaHSO4
B.NaCl
C.HCl
D.Ba(OH)2
参考答案:B
本题解析:此时c(H+)小于常温下纯水电离产生的c(H+),说明水的电离受到了抑制,NaHSO4、HCl、Ba(OH)2对水的电离都起抑制作用。
本题难度:一般
2、选择题 下列说法正确的是
A.CH4(g) + 3/2O2(g) == CO(g) +2H2O(l) ΔH== -a kJ・mol―1 ,这里ΔH代表燃烧热
B.在250C、101kPa,1mol硫和2mol硫的燃烧热相等
C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应
D.101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热
参考答案:B
本题解析:甲烷完全燃烧生成一氧化碳不是稳定的产物,能继续燃烧生成二氧化碳,A错误;燃烧热是指1mol可燃物完全燃烧生成稳定产物所放出的热量,1mol硫和2mol硫的燃烧热相等,B正确;所以可燃物的燃烧是放热的,C错误;1mol碳完全燃烧生成稳定产物所放出的热量为燃烧热,D错误,答案选B
考点:燃烧热的定义
本题难度:一般
3、填空题 A、B、C三种一元弱酸的浓度均为0.1 mol・L-1,在室温下,A溶液中C(OH-)=7.6×10-12 mol・L-1,B溶液中水电离产生的H+浓度为10-10 mol・L-1,C溶液的pH=3,则三种溶液的酸性由强到弱的顺序是______________________________。
参考答案:A>C>B
本题解析:A溶液中c(H+)=1.3×10-3 mol・L-1,B溶液中c(OH-)=10-10 mol・L-1,c(H+)=10-4 mol・L-1,C溶液中c(H+)=10-3 mol・L-1,因A、B、C浓度相同,电离产生的c(H+)越大,酸越强。
本题难度:简单
4、选择题 常温下,对于1 L 0.005 mol・L-1硫酸表述中正确的是( )
A.由水电离出的c(H+)=1.0×10-12 mol・L-1
B.加水稀释后,溶液中所有离子的浓度均减少
C.2c(H+)=c(SO42-)+c(OH-)
D.滴加稀氨水使pH=7,则c(NH4+)=c(SO42-)
参考答案:A
本题解析:A项,硫酸电离出的c(H+)=10-2 mol・L-1,所以c(H+)水=1.0×10-12 mol・L-1正确;B项,加水稀释后,c(OH-)增大,错误;C项,H2SO4=2H++SO42-,H2O H++OH-,所以c(H+)=2c(SO42-)+c(OH-),错误;D项,根据电荷守恒判断,错误。
H++OH-,所以c(H+)=2c(SO42-)+c(OH-),错误;D项,根据电荷守恒判断,错误。
本题难度:一般
5、选择题 在25℃时,向50.00 mL未知浓度的CH3COOH溶液中逐滴加入0.5 mol・L-1的NaOH溶液。滴定过程中,溶液的pH与滴入NaOH溶液体积的关系如图所示,则下列说法中,正确的是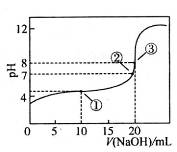
A.该中和滴定过程,最宜用石蕊作指示剂
B.图中点②所示溶液中,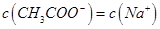
C.图中点①所示溶液中水的电离程度大于点③所示溶液中水的电离程度
D.滴定过程中的某点,会有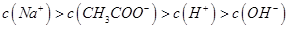 的关系存在
的关系存在
参考答案:B
本题解析:A、石蕊颜色变化不明显,不能用作酸碱中和滴定的指示剂,错误;B、图中点②pH=7,根据溶液呈中性,可得c(H+)+c(Na+)=c(CH3COO?)+c(OH?),可得c(CH3COO?)=c(Na+),正确;C、图中点①pH为4,H+浓度为10-4mol?L?1,抑制了水的电离,点③pH=8,OH?浓度为10-6mol?L?1,抑制水的电离作用较弱,所以图中点①所示溶液中水的电离程度小于点③所示溶液中水的电离程度,错误;D、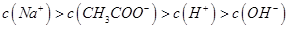 违背了电荷守恒,错误。
违背了电荷守恒,错误。
本题难度:一般