时间:2017-07-10 18:20:48
1、选择题 观察下列模型并结合有关信息,判断有关说法正确的是
| ? | 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl |
| 结构模型示意图 | 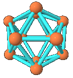 | 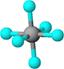 | 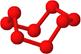 | 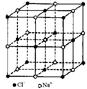 |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
参考答案:B
本题解析:A.单质硼属原子晶体,其结构单元B12中含有30个B-B键,含20个正三角形。错误。B.SF6是由极性键构成的非极性分子。正确。C.固态硫S8属于分子晶体。错误。D.NaCl是离子晶体。在熔化和溶于水均能电离产生自由移动的离子,且破坏的都是离子键,在NaCl晶胞中每个Na+周围最近且等距离的Na+有6个,分别位于该原子的上、下、左、右、前、后六个方向。正确。
本题难度:一般
2、选择题 25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g)+O2(g) ="=" 2H2O(1)△H=
参考答案:
本题解析:
本题难度:一般
3、选择题 下列电子式中,书写正确的是
参考答案:B
本题解析:氮气氮原子还有没有参与成键的电子,电子式为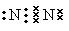 。氯化钠和氢氧化钠均是离子化合物,电子式分别为
。氯化钠和氢氧化钠均是离子化合物,电子式分别为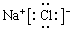 、
、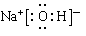 。水是由极性键形成的共价化合物,所以正确的答案是B。
。水是由极性键形成的共价化合物,所以正确的答案是B。
本题难度:一般
4、选择题 下列化合物中,既含有离子键,又含有非极性共价键的是 (? )
A.CaO
B.SiO2
C.NH4Cl
D.Na2O2
参考答案:D
本题解析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间
容易形成共价键,据此可知,A中含有离子键,B中含有极性键,C中含有离子键和极性键,D中含有离子键和非极性键,答案选D。
点评:该题是高考中的常见题型和考点,属于基础性试题的考查。试题难度不大,侧重对学生基础知识对巩固和训练,有助于培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确化学键的含义,然后灵活运用即可。
本题难度:简单
5、选择题 下列说法正确的是(? )
A.如图可表示水分解过程中的能量变化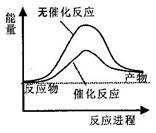
B.若2C(s)+O2(g)=2CO(g)△H="-221.0" kJ/mol,则碳的燃烧热为110.5 kJ/mol
C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D.已知:Ⅰ:对于反应:H2(g)+Cl2(s)="2HCl" (g)△H="-" a kJ/mol,
Ⅱ:
且a、b、c均大于零,则断开1molH-Cl键所需的能量为- a-b-c
参考答案:A
本题解析:图中产物的能量高于反应物的能量,为吸热反应,故可以表示水分解的能量变化;B中碳的燃烧热应该是生成物为CO2;碳的燃烧是放热反应,但需要加热,故C错误;断开1molH-Cl键所需的能量为 (a+b+c)/2,故D错
本题难度:一般