ʱ��:2017-07-10 18:13:20
1������� �״���CH3OH���Ͷ����ѣ�CH3OCH3������Ϊ21���͵�����ȼ�ϣ����й㷺�Ŀ�����Ӧ��ǰ������CH4��H2OΪԭ���Ʊ������Ѻͼ״��Ĺ�ҵ�������£�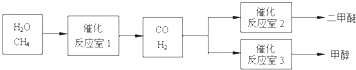
����գ�
��1����ҵ��һ������������ַ�Ӧ�ɼ״���
��Ӧ��CO��g��+2H2��g���TCH3OH��g����H1
��Ӧ��CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H2
������Ӧ���ϡ�ԭ�Ӿ��á�ԭ�����______�������
��2����һ�������£���֪��Ӧ��2�Ŀ��淴Ӧ�����ɶ����������������CO2���仯ѧ����ʽΪ______��
��3��������ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g��+CO��g��?CH3OH��g����H=-90.8kJ?mol-1
��2CH3OH��g��?CH3OCH3��g��+H2O��g����H=-23.5kJ?mol-1
��CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.3kJ?mol-1
��Ӧ��3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g����H=______kJ/mol��
��4��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ1��ʾ�ĵ��װ�ã���õ�������ĵ缫��ӦΪ��______��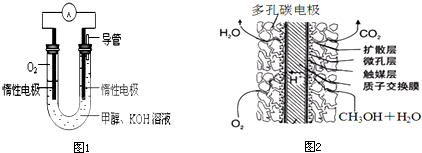
��5���״����ӽ���Ĥȼ�ϵ�أ���ͼ2��ʾ������������ҺΪ�������Һ���״���һ���缫ͨ�룬O2����һ�缫ͨ�룬�м�Ϊ���ӽ���Ĥ��ͨ��״���һ���缫��ӦʽΪ��______��
2��ѡ����
��֪�Ȼ�ѧ����ʽ��
��CO��g�� +1/2 O2 ��g����CO2 ��g�� ��H=-283.0kJ��mol-1
��H2��g�� +1/2O2 ��g�� ��H2O��g������H=-241.8 kJ��mol-1
������˵����ȷ����

3��ѡ���� ��֪C��s����H2��g����CH3COOH��l����ȼ���ȷֱ���393.5kJ/mol��285.8kJ/mol��870.3kJ/mol����ע��CH3COOH��ȼ�ղ�����CO2��H2O����Ӧ2C��s��+2H2��g��+O2��g��=CH3COOH��l���ġ�HΪ��������
A��-488.3KJ?mol-1
B��-762.6kJ?mol-1
C��-654.9kJ?mol-1
D��+191kJ?mol-1
4������� ����֪��H2(g)+1/2O2(g)=H2O(1) ��H=-285. 8kJ��mol-1��H2(g)=H2(1) ��H=0.92kJ��mol-1��O2(g)=O2(l)
��H=-6.84kJ��mol-1����д��Һ���Һ������Һ̬ˮ���Ȼ�ѧ����ʽ��_____________________��
���йؼ����������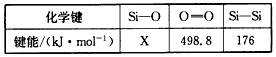
�������������ȼ�յ��Ȼ�ѧ����ʽ��Si(s)+O2(g)=SiO2(s) ��H=-989.2kJ��mol-1����Si-O���ļ���X��ֵΪ____________kJ��mol-1��
5��ѡ���� ��298K��100kPaʱ����֪���з�Ӧ
2H2O(g) = O2(g) + 2H2(g) ��H1
Cl2(g) + H2(g) = 2HCl(g) ��H2
O2(g) +4HCl(g) =2Cl2(g) + 2H2O(g) ��H3
��H3�릤H1�ͦ�H2��Ĺ�ϵ��ȷ����
[? ]
A����H3=-��H1+2��H2
B����H3=-��H1+��H2
C����H3=-��H1-2��H2
D����H3=-��H1-��H2