ʱ��:2017-07-10 17:44:21
1��ѡ���� ����H2SO4��Ba(OH)2��Na2CO3����ˮ4����Һ������ͼ��ʾ�����ϵ��ͼ��ÿ���߶����˵����ʿ��Է�����ѧ��Ӧ�������ƶϺ�������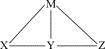
A��Mһ����Ba(OH)2
B��Y��������ˮ
C��Xһ����Na2CO3��Һ
D��Z������H2SO4
�ο��𰸣�D
�������������������4�����ʣ�Na2CO3��Ba(OH)2���ܹ�������3�����ʷ�Ӧ����Na2CO3��Ba(OH)2�ֱ�ΪM��Y�е�һ�֡���H2SO4����ˮ���ܹ���Na2CO3��Ba(OH)2��Ӧ���Ҷ��߲��ܷ�Ӧ����H2SO4����ˮ�ֱ�ΪX��Z�е�һ�֡�����������D����ȷ��
�����Ѷȣ�һ��
2��ѡ���� X��Y��Z?���ַǽ���Ԫ�ؾ�����ͬ�ĵ��Ӳ��������ǵ���̬�⻯����ȶ��Ե�ǿ��˳��Ϊ��XH3��H2Y��HZ������˵������ȷ���ǣ�������
A��ԭ��������X��Y��Z
B���ǽ����ԣ�X��Y��Z
C��ԭ�Ӱ뾶��X��Y��Z
D�����ӵĻ�ԭ�ԣ�X3-��Y2-��Z-
�ο��𰸣�A��X��Y��Z?���ַǽ���Ԫ�ؾ�����ͬ�ĵ��Ӳ���˵��X��Y��ZΪͬһ���ڣ�ͬһ����Ԫ����̬�⻯����ȶ�������ǿ����̬�⻯����ȶ��Ե�ǿ��˳��Ϊ��XH3��H2Y��HZ����ԭ������ΪX��Y��Z����A����
B��ͬһ���ڴ����ҷǽ���������ǿ���ʷǽ�����ΪX��Y��Z����B��ȷ��
C��ͬһ���ڴ����ң�ԭ�Ӱ뾶��С����ԭ�Ӱ뾶X��Y��Z����C����
D��ͬһ���ڴ�����Ԫ��ԭ�ӵ���������ǿ����Ӧ���ӵĻ�ԭ����������ԭ��X3-��Y2-��Z-����D����
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� ����Ԫ���н�������ǿ���ǣ�������
A��K
B��Na
C��Al
D��Mg
�ο��𰸣�Na��Mg��Al����ͬһ���ڣ�ԭ��������������ͬ����������ң�Ԫ�صĽ����Լ������ʽ�����Na��Mg��Al��Na��K����ͬһ���壬���Ӳ����ʽ�����K��Na��
�ʽ�����K��Na��Mg��Al��
��ѡA��
���������
�����Ѷȣ���
4��ѡ���� ����˵����ȷ����
A���ع��ͺͿ����Ͷ�������������
B�����¼����������ۻ������������䣬˵����������һ�����ܵ���������Ĥ
C��Ϊ�ⶨ�����������Ƶĵ����ԣ����������ƹ������ʯӢ�����м����ۻ�
D�����Ӻ�ˮ�еõ����Ȼ�þ��Һ�ɻ�ý���þ
�ο��𰸣�B
���������A�������͵���Ҫ�ɷ��������࣬����B�����¼����������ۻ�����������䣬����Ϊ���ɱ�Ĥ�����������۵���������۵㣬�������棬�����ۻ��˵�Һ̬��������䣬��ȷ��C��ʯӢ�����к��ж������裬�����������Ʒ�Ӧ���ɹ����ƣ�����D������Ȼ�þ��Һ���ܵõ�����þ��Ӧ��������Ȼ�þ������ѡB��
�����Ѷȣ���
5��ѡ���� ��������˳��������
A.���ԣ�H4SiO4��H3PO4��H2SO4��HClO4
B.�⻯����ȶ��ԣ�CH4��NH3��H2O��HF
C.���ԣ�KOH��Ca(OH)2��Mg(OH)2
D.�е㣺HI��HBr��HCl��HF
�ο��𰸣�D
�������������������ǽ�����Խǿ������������ˮ��������ԡ��⻯����ȶ���Խǿ������ѡ��AB��ȷ��ͬ��������Խǿ������������ˮ����ļ���Խǿ��C��ȷ������HF���Ӽ�����������HF�ķе����ͬ����Ԫ���⻯��ķе㣬D����ȷ����ѡD��
���㣺����Ԫ�������ɵ�Ӧ��
������������Ҫ�ǿ���ѧ����Ԫ�������ɵ���Ϥ�˽�̶ȣ��Լ��������Ԫ�������ɽ��ʵ��������������ѶȲ�����Ĺؼ���������סԪ�������ɵľ������ݣ�Ȼ��������������ü��ɣ�����������ѧ������˼ά������
�����Ѷȣ�һ��