时间:2017-07-10 17:34:58
1、选择题 SO3分子的构型为平面三角形,它采用的杂化类型是( )?
A.sp杂化?
B.sp2杂化?
C.sp3杂化?
D.没有杂化,只有三个σ键
2、填空题 现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
| B元素原子的核外p电子总数比s电子总数少1 |
| C原子p轨道上成对电子数等于未成对电子数,且与A同周期 |
| D元素的族序数与周期数的差为4,且不与A元素在同一周期 |
| E位于周期表中第七列 |
| F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
3、选择题 下列化学用语正确的是
[? ]
A.甲烷的球棍模型: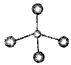
B.乙醇的分子式:CH3CH2OH
C.有18个中子的过氧化氢分子:T2O2
D.羟基的电子式: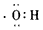
4、选择题 下列说法正确的是
[? ]
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.含有离子键的化合物一定是离子化合物
5、选择题 关于晶体的下列说法正确的是
[? ]
A.晶体中只要有阳离子,就一定有阴离子
B.晶体中只要有阴离子,就一定有阳离子
C.氢键具有方向性和饱和性,也属于一种化学键
D.金属键由于无法描述其键长、键角,故不属于化学键