ʱ��:2017-03-05 16:09:35
1��ʵ���� ��15�֣�ij��ѧ��ȤС������ʵ�����ṩ�������Լ������ۡ�0.1mol��L-1FeCl3��Һ��0.1mol��L-1FeCl2��Һ��KSCN��Һ��������ˮ��̽��Fe2+?��Fe3+�������ԡ���ԭ�ԣ�����ʵ��������Ӧ�á�
��1����ȤС��ͨ����Fe2+��Fe3+ �ļ�̬��������Fe2+��Fe3+ �������ԡ���ԭ�����������3�ּ��裺
����һ��Fe2+����?�ԣ�
�������Fe2+����?�ԣ�
��������Fe3+����?�ԣ�
��2�����ʵ�鷽��������ʵ�鲢����ʵ������������б���
| ̽������ | ʵ�鷽�� | ?ʵ������ | д���������ӷ���ʽ |
| ̽��Fe2+���л�ԭ�� | ȡ����0.1mol��L-1FeCl2��Һ����������KSCN��Һ��������Һ�м�������? | ��Һ�Ȳ���죬 ���ΪѪ��ɫ | ��Fe2+�����ķ�Ӧ�� |
| ̽��Fe3+���������� | ȡ����0.1mol��L-1FeCl3��Һ����������?��������Һ�м�������KSCN��Һ | ��Һ����ΪѪ��ɫ | ��Fe3+�����ķ�Ӧ�� |
�ο��𰸣���15�֣�����һ��Fe2+����?��ԭ?�ԣ�
�������Fe2+����?����?�ԣ�
��������Fe3+����?����?�ԣ�
��2��
̽������
ʵ�鷽��
?ʵ������
д���������ӷ���ʽ
̽��Fe2+���л�ԭ��
������Һ�м�������?������ˮ?
��Һ�Ȳ���죬���ΪѪ��ɫ
��?Fe2+�����ķ�Ӧ��
? 2Fe2++Cl2=2Fe3++ 2Cl-?
̽��Fe3+����������
��������
?����?
��Һ����ΪѪ��ɫ
��Fe3+�����ķ�Ӧ��
? 2 Fe3++ Fe= 3Fe2+?
��3���÷�Ӧ�����ӷ���ʽΪ��? Zn+Fe2+= Zn2++ Fe?��
��4����Ӧ�����ӷ���ʽ�ǣ�? 2 Fe3++Cu= 2Fe2+ +Cu2+??��
�����������
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ����
[? ]
A���Ʊ�����ú�����ԭ��֮һ����������������Ӧ
B�����ڿ����к�����ȼ��
C��þ���������Ĥ���ɣ����ܱ����ڲ����
D���������Ҫ�ɷ���Fe3O4
�ο��𰸣�A
���������
�����Ѷȣ���
3������� (12��)A��B��C��D�������ʶ�����һ�ֹ�ͬ��Ԫ�أ�A�dz����Ľ�����C����Һ���ֻ�ɫ��A��B��C��D֮����������ʾת����ϵ��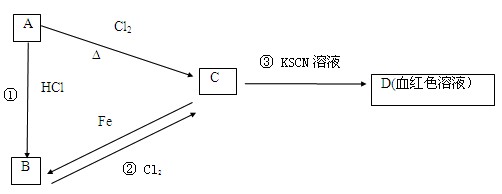
�Իش��������⣺
(1)A��?,C��?��
(2)C����Һ��NaOH��Һ��Ϻ��������??��
(3)��Ӧ�ٵķ�Ӧ������?��Ӧ��ѡ����ϡ����ֽ⡱���û��������ֽ⡱����
�ο��𰸣�(12��)
(1)A��? Fe?,C��? FeCl3?��
(2)?�������ɫ����?��
(3)?�û�?��
�����������
�����Ѷȣ�һ��
4������� ��12�֣�����Ⱦ�����ķ������ࣨ��Ҫ�ɷ���Fe2O3��FeO�������Ʊ����������ηɻ�Ϳ���������������������������Ϊ��
��ش�
��1�����̢���Ҫ��Ӧ�����ӷ���ʽΪ?��
��2����֪������������Ksp=4.87��10-17������������Ksp=2.6��10-39��
����Һ��ij����Ũ�Ȳ�����1��10-5 mol��L-1ʱ��������Ϊ�������Ѿ���ȫ������ͨ��������������˵�����̢ڵ���pH=9��ԭ����?��
��3������D����Ҫ�����������⡢������Ԫ�ص�������Ϊ56��1��32������̢���Ҫ��Ӧ�Ļ�ѧ����ʽΪ?��
��4����֪Fe2+����������Һ�л�ԭ�Խ�ǿ��ͼ11���о����̢ܵ�ʵ�����ã���÷�Ӧ�����ʱ�������?Сʱ���ң���Ϊ���ˡ�
��5��ij�������������ࣨ�����Ԫ�غ���Ϊ16.8 %��������Ϊ10��/Сʱ���������������������IJ���Ϊ4.64��/Сʱ���粻���ǹ��̢��Ժ�������Fe2+����������ù���ÿСʱ�������۵�����Ϊ?ǧ�ˡ�
�ο��𰸣���1��2Fe3+ + Fe �� 3Fe2+?��2�֣�?��2����pH=9ʱ��c(Fe2+)��4.87��10-7mol��L��1 ��2�֣�
��3��2Fe(OH)2 +H2O2��2FeO(OH)+2H2O������Dд��Fe(OH)O��FeHO2��FeO2H�����ԣ���2�֣�?��4��0.16��2�֣�?��5��560��4�֣�
�����������1����ҺA�к��������ӣ����Է���ʽΪ2Fe3+ + Fe �� 3Fe2+��
��2�������������������ܶȻ�������֪����pH��9ʱ��c(Fe2+)��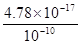 4.87��10-7mol��L��1����ʱ�Ѿ���ȫ������
4.87��10-7mol��L��1����ʱ�Ѿ���ȫ������
��3�������⡢������Ԫ�ص�������Ϊ56��1��32����ԭ�Ӹ���֮��ʱ1�U1�U2������ѧʽΪFeO(OH)�����Է�Ӧʽ��2Fe(OH)2 +H2O2��2FeO(OH)+2H2O��
��4������ͼ11��֪������Һ��������ʱ����Ӧ��ʱ���Լ��0.16h��
��5��4.64������������������������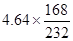 ��3.36�֣������൱����������������2.24�֣���������������������ӡ�10������������������16.8 %��10��1.68�֣�������Ҫ���۵�������2.24�֣�1.68�֣�0.56�֡�
��3.36�֣������൱����������������2.24�֣���������������������ӡ�10������������������16.8 %��10��1.68�֣�������Ҫ���۵�������2.24�֣�1.68�֣�0.56�֡�
�����Ѷȣ�һ��
5��ѡ���� �������п�ͼ����,����˵����ȷ����(����)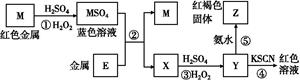
A��E3+�������Ա�M2+����������
B���ڷ�Ӧ��������ȱ��������ԡ��ֱ�����������
C����Ӧ�ܵ����ӷ���ʽ�ɱ�ʾΪ:3SCN-+E3+ E(SCN)3��
E(SCN)3��
D���ڢ۷�Ӧ��������ϡ������ܿ������ɫ����
�ο��𰸣�D
���������M�Ǻ�ɫ����,�����ȷ���ǽ���ͭ,��H2O2��������H2SO4��Ӧ����CuSO4,Y����KSCN���ֺ�ɫ,Y����Fe3+,�����E����,X��FeSO4,���۲���Ӧ����ΪFe2(SO4)3,�백ˮ��Ӧ�õ����ɫ��Fe(OH)3��Fe3+�������Ա�Cu2+��������ǿ,A��;�ڷ�Ӧ��������ֻ����������,H2O2������������,B��;SCN-��Fe3+��Ӧ���ɵIJ����ǿ�����ˮ��������,C��;��Ӧ��Ϊ:2Fe2++H2O2+2H+ 2Fe3++2H2O,�ɼ���Ӧ��������H+,pH����,�п��ܻ����ɺ��ɫ��Fe(OH)3����,D��ȷ��
2Fe3++2H2O,�ɼ���Ӧ��������H+,pH����,�п��ܻ����ɺ��ɫ��Fe(OH)3����,D��ȷ��
�����Ѷȣ�һ��