时间:2017-03-05 15:40:46
1、选择题 汽车上的催化转化器,可将尾气中的主要污染物转化成无毒物质,反应为: 在某温度时.,用气体传感器测得不同时间的NO和CO浓度如表
在某温度时.,用气体传感器测得不同时间的NO和CO浓度如表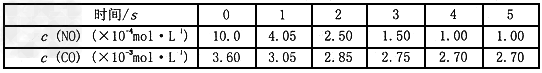
经分析,得出结论不正确的是
[? ]
A. 该反应转化较快,具有存实际意义
B. 催化转化器在冬季时对废气转化效率比夏季更高
C. 2s末的平均反应速率 ?
?
D. 在该温度下,反应的平衡常数K=5000
2、选择题 在一密闭容器中有如下反应:aX(g)+bY(g)?nW(g);△H=Q.某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图: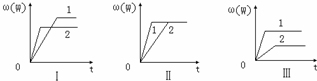
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间.其它条?件不变时,下列分析正确的是( )
(1)图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b<n
(2)图Ⅲ可能是不同温度对反应的影响,且T1>T2,△H<0
(3)图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b
(4)图Ⅱ可能是在同温同压下催化剂对反应的影响,且1中使用的催化剂效果好.
A.(1)(2)
B.(1)(3)
C.(2)(4)
D.(1)(4)
3、选择题 下列有关平衡常数的说法中,正确的是
?[? ]
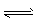 N2O4(g) △H<0,升高温度该反应平衡常数增大
N2O4(g) △H<0,升高温度该反应平衡常数增大 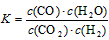 的反应,化学方程式为
的反应,化学方程式为
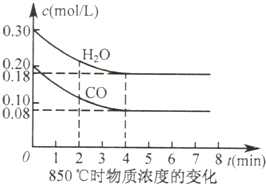
4、简答题 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如表所示:
| 温度/℃ | 400 | 500 | 850 平衡常数 9.94 9 1 |
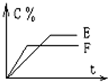
5、填空题 mA(气)+nB(气)?pC(气)+qD(气)的C%与时间t有如图关系
(1)若E、F表示两种温度,则E______F(填>、<或=),正反应______热
(2)若E、F表示两种压强,则m+n______p+q.