时间:2017-03-05 14:55:52
1、选择题 已知H2O2的分子空间结构可在二面角中表示,如图,则关于H2O2的说法正确的是(?)
A.H2O2分子的电子式为:H+[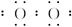 ]2-H+
]2-H+
B.H2O2分子中共含14个电子
C.H2O2是非极性分子
D.H2O2分子正、负电荷重心不重合
参考答案:D
本题解析:H2O2为共价化合物,其电子式为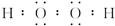 。H2O2分子中共含18个电子。由图示可知,H2O2分子的正、负电荷重心不重合,故H2O2为极性分子。
。H2O2分子中共含18个电子。由图示可知,H2O2分子的正、负电荷重心不重合,故H2O2为极性分子。
本题难度:简单
2、选择题 已知:在101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,单位为kJ/mol。下列有关热化学方程式的叙述正确的是 ( )
A.已知2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ·mol-1,则氢气的燃烧热为285.8 kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l)△H=-57.4 kJ/mol
D.己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2
参考答案:A
本题解析:A 2H2完全燃烧产生2mol的液态水,放出热量是571.6 kJ,所以产生1mol的液态水,放出热量是571.6 kJ÷2=285.8KJ,所以氢气的燃烧热为285.8 kJ/mol,正确;B.根据物质的转化可知金刚石的能量高于石墨,物质所含有的能量越低,物质的稳定性就越强,则金刚石不如石墨稳定,错误;C.由于醋酸是弱酸。电离需要吸收热量,所以稀醋酸和稀NaOH溶液反应,产生1mol的水时放出的热量小于57.4 kJ,因此反应热△H>-57.4 kJ/mol,错误;D.这两个反应都是放热反应,反应放出的热量越多,则反应热就越小,所以△H1<△H2,错误。
考点:考查反应热与物质的存在状态、物质的强弱、多少的关系的知识。
本题难度:一般
3、选择题 已知断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol H—N键吸收的能量为391 kJ,根据化学方程式:N2(g)+3H2(g)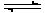 2NH3(g) ΔH=-92.4 kJ·mol-1,则断裂1 mol N≡N键吸收的能量是
2NH3(g) ΔH=-92.4 kJ·mol-1,则断裂1 mol N≡N键吸收的能量是
A.431 kJ
B.945.6 kJ
C.649 kJ
D.869 kJ
参考答案:B
本题解析:
试题解析:已知:H-H键能为436kJ/mol,H-N键能为391kJ/mol,设N≡N的键能为x,对于反应N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol,反应热=反应物的总键能-生成物的总键能,
故x+3×436kJ/mol-2×3×391kJ/mol=-92.4kJ/mol,解得:x="945.6" kJ/mol故选B.
考点:有关反应热的计算
本题难度:一般
4、选择题 已知:S(s)+O2(g)→SO2(g)+297.23kJ………………①
2SO2(g)+O2(g)  2SO3(g) +196.64kJ……②
2SO3(g) +196.64kJ……②
假设反应过程中无热量损失,则
A.1mol S(s)完全反应,并转化为SO3(g)时,放出395.55 kJ热量
B.1个SO2和1个O2分子储存的能量之和大于1个SO3分子
C.1 L SO2(g)完全反应生成1L SO3(g),放出98.32 kJ热量
D.使用催化剂,可以减少反应②放出的热量
参考答案:B
本题解析:A、根据盖斯定律可知①×2+②得到2S(s)+3O2(g)→2SO2(g)+791.1kJ,但由于反应②是可逆反应,则1mol S(s)完全反应,并转化为SO3(g)时,放出的热量小于395.55 kJ,A错误;B、反应②是放热反应,则1个SO2和1个O2分子储存的能量之和大于1个SO3分子,B正确;C、系数表示物质的量,则1 mol SO2(g)完全反应生成1mol SO3(g),放出98.32 kJ热量,C错误;D、催化剂不能改变反应热和平衡状态,因此使用催化剂,不能减少反应②放出的热量,D错误,答案选B。
考点:考查反应热的有关计算与判断
本题难度:一般
5、选择题 下列反应中,属于吸热反应的是
A.食物的腐败
B.铝与稀盐酸反应
C.二氧化碳与碳反应生成一氧化碳
D.甲烷在氧气中的燃烧
参考答案:C
本题解析:A项食物的腐败、B.铝与稀盐酸反应、D.甲烷在氧气中的燃烧均属于放热反应,故A、B、D均错误;C项二氧化碳与碳反应生成一氧化碳属于吸热反应,故C项正确。
考点:化学反应能量变化。
本题难度:简单