时间:2017-03-05 14:25:32
1、选择题 下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是
[? ]
A.NaHSO4和Ba(OH)2
B.AlCl3和NaOH
C.NaAlO2和H2SO4
D.Ba(HCO3)2和Ba(OH)2
参考答案:AD
本题解析:
本题难度:简单
2、实验题 设计实验探讨向AlCl3溶液中加入过量的NaOH和向NaOH溶液中加入过量的AlCl3现象是否一样。_________________________________
参考答案:向AlCl3溶液中逐滴加入NaOH有白色沉淀生成,当NaOH过量时沉淀溶解,最后生成物为NaAlO2。反应的离子方程式为:Al3++3OH-==Al(OH)3↓,Al(OH)3+OH-==?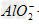 +2H2O
+2H2O
向NaOH溶液中逐滴加入AlCl3溶液时,观察到的现象是:开始有白色沉淀生成,振荡后立即消失,继续滴加AlCl3溶液直至过量时,又出现白色沉淀,且不消失。这是因为反应开始时,由于NaOH溶液过量,滴入的AlCl3和NaOH作用转化为NaAlO2,当加入过量AlCl3时,AlCl3和NaAlO2在溶液里发生反应,生成沉淀Al(OH)3。其反应的离子方程式为:Al3++3OH-====Al(OH)3↓,Al(OH)3+OH-==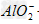 +2H2O,Al3++3
+2H2O,Al3++3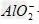 +6H2O==4Al(OH)3↓
+6H2O==4Al(OH)3↓
综上所述,二者滴加顺序不同,现象不一样。
本题解析:
本题难度:一般
3、填空题 100 mLamoI/L的AlCl3溶液与100 mL b mol/L 的NaOH溶液混合,讨论a与b在不同关系时所得沉淀的物质的量。
当___时,____;
当___时,____;
当___时,____。
参考答案:当b≤3a时,n[Al(OH)3] =0.1b/3 mol;
当3a<b<4a时,n[Al(OH)3]=(0.4a-0.1b)mol;
当 b≥4a时,n[Al(OH)3]=0。
本题解析:
本题难度:一般
4、填空题 锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为_______________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式 ____________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是____________________。(填序号)
① 硫酸铝和氢氧化钠 ② 硫酸铝和氨水③ 硫酸锌和氢氧化钠④ 硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式 __________________________。试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因_______________________
参考答案:(1)AlO2-(或Al(OH)4-)
(2)Zn+2NaOH==Na2ZnO2+H2↑ (或Zn+2NaOH+2H2O==Na2Zn(OH)4+H2↑)
(3)①③④
(4)Al3++3NH3・H2O==Al(OH)3↓+3NH4+;可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水中,生成Zn(NH3)42+,氨水的用量不易控制
本题解析:
本题难度:一般
5、选择题 在含有少量盐酸的AlCl3溶液中逐滴加入过量的氨水至溶液呈碱性,下图中,能表示该反应产生的沉淀的质量m与加入氨水的体积V关系的是
[? ]
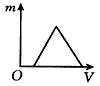
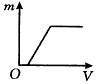
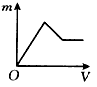
参考答案:C
本题解析:
本题难度:一般