时间:2017-03-05 14:22:54
1、选择题 已知C(s)、H2(g)、CH3COOH(l)的燃烧热分别是393.5kJ/mol、285.8kJ/mol和870.3kJ/mol,(注:CH3COOH的燃烧产物是CO2和H2O)则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的△H为( )
A.-488.3KJ?mol-1
B.-762.6kJ?mol-1
C.-654.9kJ?mol-1
D.+191kJ?mol-1
参考答案:A
本题解析:
本题难度:一般
2、填空题 已知下列两个反应:
a.C2H2(g)+H2(g)=C2H4(g) ΔH<0
b.2CH4(g)=C2H4(g)+2H2(g) ΔH>0
判断以下3个热化学方程式ΔH1、ΔH2、ΔH3由大到小的顺序是__________________________________。 ①C(s)+2H2(g)=CH4(g) ΔH1
②C(s)+1/2H2(g)=1/2C2H2(g) ΔH2
③C(s)+H2(g)=1/2C2H4(g) ΔH3
参考答案:
ΔH1<ΔH3<ΔH2
本题解析:
本题难度:一般
3、简答题 I.高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1
②C(石墨)+CO2(g)=2CO(g)△H2,则△H=______(用含△H1、△H2代数式表示)
(2)高炉炼铁反应的平衡常数表达式K=______.
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 甲/mol 1.0 1.0 1.0 1.0 乙/mol 1.0 1.5 1.0 1.0 |
| 编号 | 温度/K | 反应时间/h | 反应物物质的量配比 | 实验目的 ① 378 3 3:1 | 实验②和④探究______ 实验②和______探究反应时间对产率的影响 ② 378 4 4:1 ③ 378 3 ______ ④ 398 4 4:1 |
参考答案:I.(1)①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1①
C(石墨)+CO2(g)=2CO(g)△H2②
由①-②×3,得到热化学方程式:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=△H1-3△H2,
故答案为:△H1-3△H2;
(2)反应Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)的平衡常数K=c3(CO2)c3(CO),故答案为:c3(CO2)c3(CO);
(3)①令平衡时CO的物质的量变化为nmol,则:
Fe2O3(s)+3CO(g)?Fe(s)+3CO2(g)
开始(mol):11 1 1
变化(mol):nn n n
平衡(mol):1-n 1-n n n
所以K=c3(CO2)c3(CO)=n3(CO2)n3(CO)=n3(1-n)3=64,解得n=0.6,所以CO的平衡转化率为0.6mol1mol×100%=60%,故答案为:60%;
②②A、该反应是反应前后气体体积没有变化的反应,容器中的压强不再发生变化,不能证明达到了平衡状态,故A错误;
B、该容器的体积保持不变,根据质量守恒定律知,反应前后混合气体的质量会变,所以容器内气体的密度会变,当容器中气体的密度不再发生变化时,能表明达到化学平衡状态,故B正确;
C、该反应是反应前后气体体积没有变化的反应,增加反应物气体的物质的量平衡不发生移动,转化率不变,故C错误;
D、氧化铁是固体,增加Fe2O3的量,不影响平衡移动,故D错误;
故选:B.
II.实验根据控制变量法进行对比试验,研究温度、反应时间、反应物配比对氧化镁产率的影响.
实验①和③,温度相同,反应时间相同,应研究反应物配比对氧化镁产率的影响,③中反应物配比应为4:1;
实验②和④,反应时间相同,反应物配比相同,温度不同,应是探究温度对产率的影响;
③中反应物配比应为4:1,实验②和③,温度相同、反应物配比相同,反应时间不同,探究反应时间对产率的影响.
故答案为:4:1;温度对产率的影响;③;
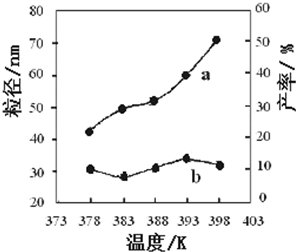
由图表中数据可知,在378K~398K,纳米MgO的粒径大小无明显变化,在383K较低温度下有利于形成较小的颗粒,纳米MgO产率随温度的升高而增大.
故答案为:在378K~398K,纳米MgO的粒径大小无明显变化,在383K较低温度下有利于形成较小的颗粒,纳米MgO产率随温度的升高而增大.
本题解析:
本题难度:一般
4、填空题 热化学方程式中的H实际上是热力学中的一个物理量,叫做焓。一个体系的焓(H)的绝对值到目前为止还没有办法测得,但当体系发生变化时,我们可以测得体系的焓的变化,即焓变,用“ΔH”表示,ΔH=H(终态)-H(始态)。
(1)化学反应中的ΔH是以_______?的形式体现的。对于化学反应A+B=C+D,若H(A)+H(B)>H(C)+H(D),则该反应的ΔH为____0(填“大于”.“小于”),该反应是?_____(填“放热”或“吸热”)反应。?
(2)进一步研究表明,化学反应的焓变与反应物和生成物的键能有关。?
已知:298K时,
H2(g)+Cl2(g)=2HCl(g)?ΔH=?-185?kJ/mol?ΔH(H2)=?436?kJ/mol, ΔH(Cl2)=?247?kJ/mol。?则ΔH(HCl)=?________________。
(3)Hess?G.H在总结大量实验事实之后认为,只要化学反应的始态和终态确定,则化学反应的ΔH便是定值,与反应的途径无关。这就是有名的“Hess定律”。
已知:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)?ΔH?=?-25?kJ/mol?
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)?ΔH?=?-47?kJ/mol?
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)?ΔH?=?+19?kJ/mol
请写出CO还原FeO的热化学方程式_______________________。?
参考答案:(1)热能;小于;放热?
(2)434 kJ/mol
(3)FeO(s)+CO(g)==Fe(s)+CO2(g)? △H= -11 kJ/mol
本题解析:
本题难度:一般
5、选择题 如下图所示,△H1=-393.5 kJ/mol,△H2=-395.4 kJ/mol,下列说法或表示式正确的是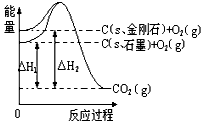
[? ]
A.C(s、石墨)== C(s、金刚石) △H=+1.9 kJ/mol
B.石墨和金刚石的转化是物理变化
C.金刚石的稳定性强于石墨
D.1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
参考答案:A
本题解析:
本题难度:一般